au sommaire
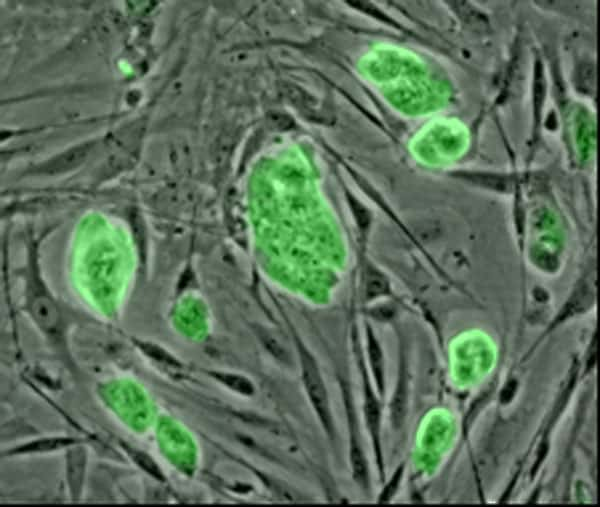
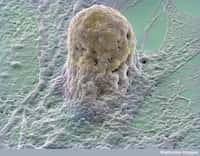
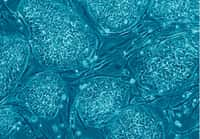
Les cellules souches ont la particularité de se différencier en n'importe quel tissu et ouvrent des perspectives considérables dans la médecine régénérative. Grâce au Prochymal, elles pourraient soigner les 3.500 à 4.000 patients atteints de réaction aiguë du greffon contre l'hôte, ou GVHD. © National Science Foundation, Wikipédia, DP
La médecine régénérative n'en est encore qu'à ses balbutiements. Si les thérapies à base de cellules souches commencent à se faire une place dans les essais cliniques, elles ne sont pas encore banalisées dans la population. Mais leur heure sonnera peut-être bientôt, car Santé Canada, ministère en charge des affaires sanitaires dans le pays, vient d'accepter, sous conditions, la mise sur le marché du premier médicament à base de cellules souches.
Le Prochymal, produit par le laboratoire américain Osiris Therapeutics, sera administré aux enfants atteints d'une maladie rare, nommée réaction aiguë du greffon contre l'hôte (GVHD en anglais), chez qui les autres traitements, à base de stéroïdesstéroïdes notamment, auront été inefficaces. Elle se produit lorsque le receveur d'une greffe de moelle osseuse est victime d'agression par les lymphocytes d'un donneur incompatible. Les symptômessymptômes sont variés et se manifestent par des douleursdouleurs abdominales, la chute de cheveux, des troubles digestifs et pulmonaires, entre autres, et s'avère mortelle chez 80 % des enfants. Jusque-là, on ne pouvait proposer aucune alternative à ces malades.
Prochymal, un médicament sous conditions
Cependant, les autorités sanitaires canadiennes ont exigé du laboratoire qu'il poursuive les tests sur son médicament durant quelques années après sa mise en circulation. En effet, deux essais cliniques menés en 2009 avaient démontré qu'il n'était pas plus efficace qu'un placéboplacébo pour traiter les patients atteints de GVHD. À l'exception d'une sous-population de malades, affectés par les formes sévères.
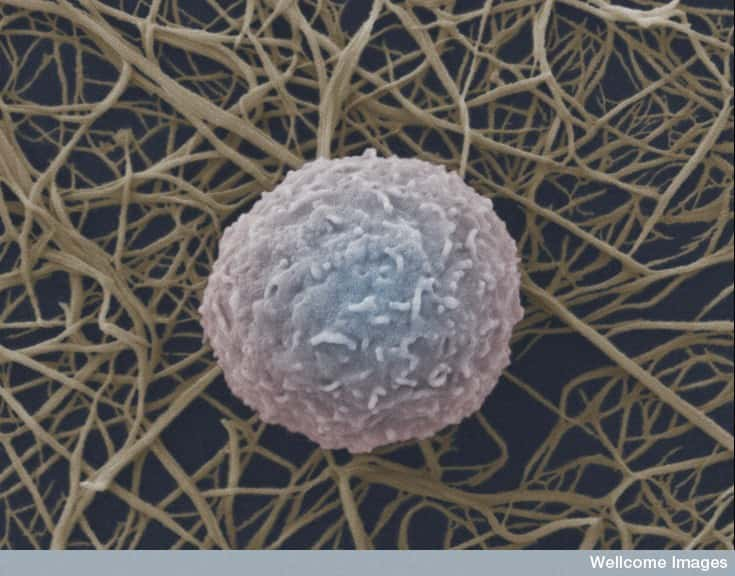
Les globules blancs, dont font partie les lymphocytes, sont des cellules du système immunitaire fabriquées dans la moelle osseuse. Dans le cas d'une greffe de cet organe, elles peuvent agresser le corps du receveur, puisqu'il est étranger à ces cellules. C'est la cause de la réaction aiguë du greffon contre l'hôte. © Anne Weston, Wellcome Image, Flickr, cc by nc nd 2.0
En amassant et en regroupant toutes les données émanant des différents essais menés depuis, Osiris Therapeutics a démontré à Santé Canada que le Prochymal fournissait des résultats cliniques significatifs chez 61 à 64 % des personnes atteintes de GVHD qui ne répondaient pas aux autres traitements, après 28 jours de thérapie. De plus, le médicament augmente le taux de survie de ces enfants.
Désormais, le laboratoire veut conquérir le marché américain, il a prévu de s'entretenir avec la Food and Drug AdministrationFood and Drug Administration (FDA)), l'agence américaine du médicament, dans les douze mois à venir. En règle générale, la FDA n'approuve pas un médicament lorsque celui-ci ne montre des effets que pour une sous-population de malades. L'absence de thérapies équivalentes la poussera-t-elle à faire une exception ?
Les médicaments avec cellules souches prêts à conquérir le marché
Le Prochymal se compose de cellules souches de moelle osseuse récupérées chez des donneurs adultes en bonne santé. Après mise en culture, un seul donneur suffit à fournir 10.000 doses. Le médicament est conçu pour contrôler les réactions inflammatoires, promouvoir la régénération tissulaire mais aussi prévenir la formation de cicatrices. Les mécanismes d'action ne sont pourtant pas encore bien maîtrisés.
S'il est le premier à recevoir la précieuse AMM (autorisation de mise sur le marchéautorisation de mise sur le marché), la concurrence n'est pas absente pour autant. Le laboratoire Althersys Inc reconnaît avoir rencontré la FDA le mois dernier pour évoquer les résultats d'essais cliniques tout juste terminés, qui portaient sur un médicament appelé MultiStem. Également à base de cellules souches, il vise à soigner les malades du GVHD traités pour des leucémiesleucémies ou d'autres conditions de la moelle osseusemoelle osseuse, qui rendent ces patients à risque de complications.
En tout, des dizaines de thérapies basées sur les cellules souches sont en cours d'essais cliniques. Cette annonce devrait sûrement inciter de nouveaux laboratoires à tester leurs produits. Au fur et à mesure, ces médicaments pourraient bien se faire une place dans les rayons des pharmacies !