au sommaire
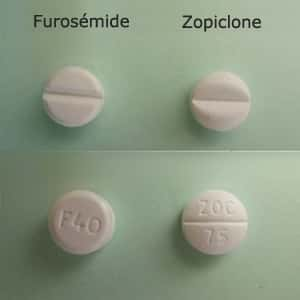
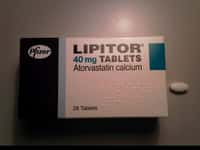
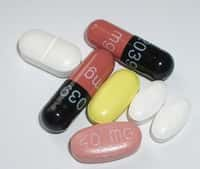
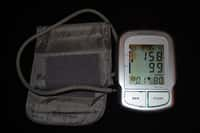
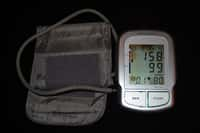
Le Furosémide Teva (un diurétique) et le Zopiclone Teva (un somnifère) se ressemblent beaucoup sous la forme de comprimés. Bien que la différence puisse être faite entre les deux, l'ANSM demande à ce que tous les diurétiques du laboratoire Teva soient rapportés chez le pharmacien. © ANSM
Après le retrait vendredi de deux lots de Furosémide Teva 40 mg et le décès d'un patient, l'Agence nationale de sécurité du médicament et des produits de santé (ANSM)) a dépêché ce lundi quatre contrôleurs dans l'usine de Sens (Yonne). Par ailleurs, l'erreur de conditionnement pourrait être responsable d'un nouveau décès et d'une hospitalisation. Par mesure de précaution, l'ANSM demande aux patients de rapporter chez leur pharmacienpharmacien toutes les boîtes qui leur auraient été délivrées, sans distinction de numéro de lot.
L'agence du médicament a reçu lundi matin « deux nouveaux signalements de pharmacovigilance (un décès et un cas grave) », fait-elle savoir par un communiqué. Une Compiégnoise (Oise) de 101 ans est décédée et une patiente de 73 ans est en réanimation à Tours (Indre-et-Loire). « Pour l'un des cas, le patient semble avoir été traité par le produit incriminé (lots Y175 ou Y176) retiré de la vente vendredi. Des investigations sont encore en cours concernant le dernier signalement, afin de déterminer le lot administré. D'autres signalements sont actuellement à l'étude. »

Quelle est la cause de cette erreur de conditionnement pour le Furosémide Teva ? Pour l'heure, on l'ignore encore. L'enquête tentera de faire la lumière sur cette histoire. © David Richfield, Wikimedia Commons, cc by sa 3.0
L’enquête se poursuit sur la mort du nonagénaire marseillais
L'ANSM avait signalé dimanche « le décès d'une personne âgée de 91 ans dont le traitement comportait entre autres du Furosémide ». L'agence a été avertie de l'ouverture d'une enquête judiciaire à Marseille à ce sujet. À ce stade, « il n'est pas possible d'établir un lien de causalité entre le décès de ce patient et le problème de conditionnement signalé sur la base des éléments dont nous disposons actuellement, insiste-t-elle. C'est l'enquête judiciaire qui déterminera l'imputabilité. »
« Suite à l'identification d'un problème de conditionnement, des comprimés de Furosémide [ont pu] être remplacés ponctuellement dans les blisters par des comprimés de Zopiclone Teva, indiquait dès vendredi l'ANSM. Cette substitution [a pu] entraîner un risque de somnolence pour le patient mais également un manque d'effet diurétique. »
Ainsi, un malade qui prendrait un somnifère à la place d'un diurétique s'exposerait naturellement à une somnolence. Il risquerait même de s'endormir quelques heures, parfois plus longtemps chez des personnes âgées ou sensibles. « Les conséquences peuvent être des chutes entraînant des fractures et traumatismes. Pour les conducteurs de véhicules, il y a un risque d'accident par somnolence ou perte de vigilance », explique l'ANSM.
Toutes les boîtes de Furosémide Teva à remettre au pharmacien
Par ailleurs, « le Furosémide Teva 40 mg (générique du Lasilix 40 mg) est prescrit en cas d'œdèmesœdèmes, d'insuffisance cardiaque ou d'hypertension artérielle », rappelle l'agence. Or sans traitement, « ces œdèmes peuvent augmenter assez rapidement. Une poussée d'insuffisance cardiaqueinsuffisance cardiaque peut survenir. La reprise du traitement par diurétique doit donc être effectuée rapidement et permet de remédier à ces risques ».
En accord avec l'ANSM, le laboratoire Teva Santé avait décidé de procéder au rappel de deux lots issus de la même campagne de production de la spécialité Furosémide Teva 40 mg, comprimé sécable (CIP 34009 361 452 4 5) :
- lot Y175 (exp 08/2015)
- lot Y176 (exp 08/2015)
Il est à présent demandé aux patients de retourner les boîtes de Furosémide Teva, quel que soit le lot. Pour plus d'informations, contactez le numéro vert (appel gratuit depuis un poste fixe) du laboratoire Teva Santé, 24h/24 : 0 800 51 34 11.