C’est le Graal des chimistes depuis des dizaines d’années : obtenir un anneau composé uniquement d’atomes de carbone reliés chacun à deux autres. Un exploit qu’a enfin réussi une équipe de chercheurs de l’université d’Oxford et d’IBM Research, en manipulant les atomes un à un sans faire s’effondrer la structure. Ce cyclocarbone devrait théoriquement avoir des propriétés fantastiques pour un nouveau type d’électronique.
au sommaire
Le carbone est l'un des éléments les plus abondants sur Terre, mais il se présente sous des formes radicalement différentes selon la configuration de ses atomes (allotropesallotropes). Sa forme amorpheamorphe, le charboncharbon, est une structure désordonnée. Lorsqu'un atome de carbone est lié à trois autres dans une structure hexagonale, on obtient du graphite. Ajoutez une liaison supplémentaire et vous avez du diamant, un matériau « ultradur ». Dans les années 1985, sont apparus les fullerènes -- une sorte de « ballonballon de football » composé de feuilles d'anneaux hexagonaux ou pentagonaux --, puis les nanotubes de carbonesnanotubes de carbones, des feuilles de graphite enroulées, et enfin le fameux graphène, une fine feuille bidimensionelle de graphite.
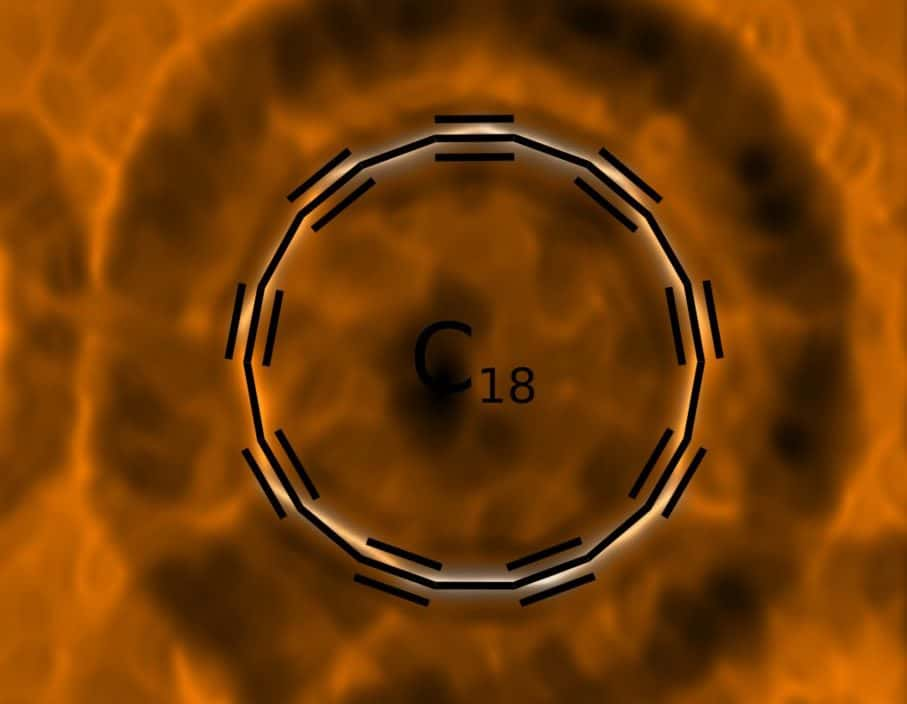
L’existence de cyclocarbone théorisée depuis des dizaines d’années
Mais, est-il possible de créer un anneau de carbone, où chaque atome serait lié à seulement deux autres ? Depuis les années 1960, de nombreux chimistes, comme le prix Nobel Roald Hoffmann, ont depuis des années théorisé l'existence d'une telle structure nommée cyclocarbone. Dans cette configuration, chaque atome de carbone peut former soit une double liaison de chaque côté -- les atomes adjacents partageant deux électronsélectrons -- soit une triple liaison d'un côté et une simple liaison de l'autre. Diverses équipes ont tenté de synthétiser des anneaux ou des chaînes à partir de ce modèle. Le problème est que ce type de structure est très réactifréactif et bien moins stable que le graphènegraphène ou le diamant. On doit donc ajouter d'autres atomes que le carbone afin de le rendre moins réactif. Certaines tentatives ont bien abouti à la création de cyclocarbones en phase gazeuse, mais avec une duréedurée de vie bien trop fugace pour étudier les liaisons entre les atomes de carbone.
Supprimer un à un les groupes CO du précurseur pour obtenir du carbone pur
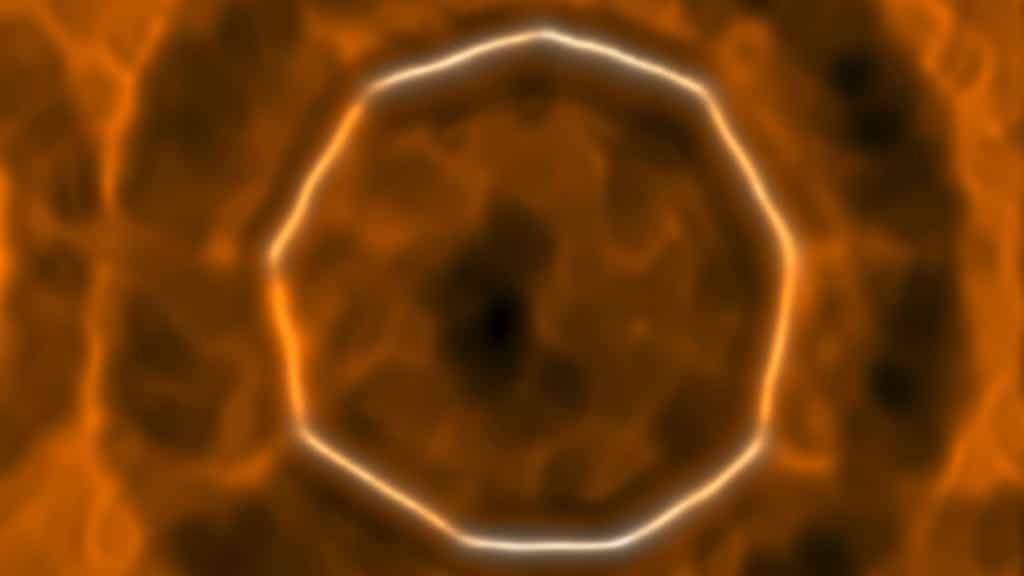
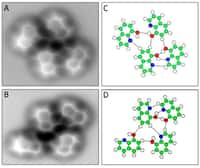
Aujourd'hui, il semble que le fameux anneau soit enfin devenu réalité, grâce à une équipe de l'université d'Oxford et d'IBMIBM Research. Dans un article publié le 15 août dans la revue Science, les chercheurs affirment avoir produit un cercle composé uniquement de 18 atomes de carbone. Cela n'a pas été chose simple. Les chercheurs sont partis d'un précurseur, l'oxyde de cyclocarbone triangulaire (C24O6). Il s'agit de 18 atomes de carbone liés à 6 moléculesmolécules de monoxyde de carbonemonoxyde de carbone, regroupés à chacun des trois coins du triangle. La molécule a été transférée sur une couche de chlorure de sodiumsodium se trouvant sur une plaque de cuivrecuivre refroidie dans une chambre à vide, ce qui permet d'obtenir une surface inerte maintenant la structure stable.
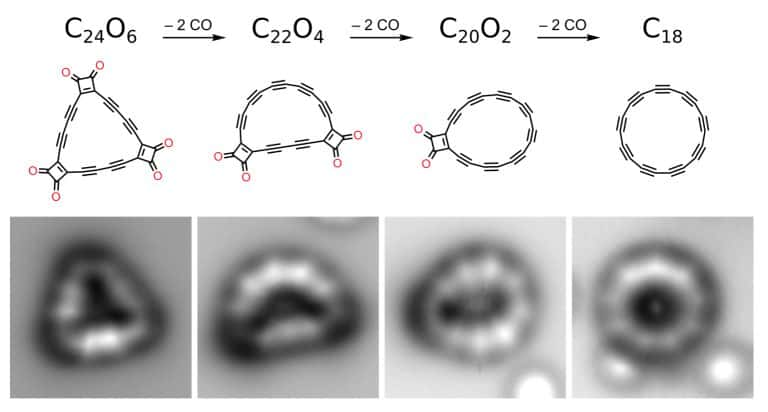
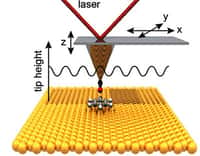
Ils ont ensuite utilisé un microscope à force atomiquemicroscope à force atomique pour retirer un à un les 6 groupes CO du C24O6. Une procédure extrêmement délicate : dans de nombreux cas, la structure s'est effondrée et les efforts des chercheurs n'aboutissant qu'à des molécules type C22O4 et C20O2. Finalement, ils sont parvenus à obtenir un C18 parfait, avec une alternance de liaisons doubles et de liaisons triples. « Je n'aurais jamais pensé y arriver un jour », a avoué Lorel Scriven, chimiste à l'université d'Oxford et co-auteur de l'article.
Des circuits électroniques à un seul électron
Mais pourquoi le cyclocarbone intéresse-t-il tant les scientifiques ? Théoriquement, une chaîne de carbone avec une telle alternance de liaisons devrait avoir des propriétés de semi-conducteursemi-conducteur et pourrait servir à la fabrication de transistors de taille moléculaire. Un circuit électronique à un seul électron ouvrirait la voie à une électronique à très faible puissance et au calcul neuromorphique. Cependant, les applicationsapplications concrètes sont encore loin : pour l'instant, chaque anneau doit être synthétisé un par un. L'équipe va donc à présent plancherplancher sur un moyen de produire plusieurs cyclocarbones en même temps, mais aussi sur l'obtention d'autres allotropes de carbone ou d'autres composés chimiques via le même processus que celui utilisé pour leur expérience.
Making and Imaging Cyclocarbon © IBM Research blog
Ce qu’il faut
retenir
- Les chimistes essayent depuis des dizaines d’années de fabriquer des anneaux de carbone pur baptisés cyclocarbones.
- Des chercheurs de l’université d’Oxford et d’IMB Research sont parvenus à produire un cyclocarbone C18 avec une alternance de liaisons doubles et triples.
- Cette structure permettrait théoriquement d’obtenir des semi-conducteurs de taille moléculaire.