En appliquant une solution d’urée à un blanc d’œuf dur et en le centrifugeant, des scientifiques ont pu rétablir la protéine appelée lysozyme. Une expérience étonnante et qui, malgré les apparences, est loin d’être inutile.
au sommaire
Lorsqu'un œuf cuit, les protéinesprotéines se déroulent, coagulent et l'œuf durcit. Ce processus apparemment irréversible peut-il être inversé ? Un plat raté peut-il être recommencé avec les mêmes ingrédients ? Des scientifiques de l'université d'Irvine (Californie) et d'Adélaïde(Australie) publient dans la revue ChemBioChem un protocoleprotocole avec lequel ils ont réussi à« décuire» un œuf. Matériel nécessaire : une solution d'urée et une machine innovante qui centrifuge -- pas l'idéal pour la cuisine.

Mais l'expérience n'est pas si anecdotique qu'elle n'y paraît. En réalité, ce procédé pourrait révolutionner la production industrielle de protéines, et baisser les coûts de nombreux traitements, comme des anti-cancéreux. Zoom sur cette technique rapide, efficace et peu coûteuse.
Le lysozyme du blanc d'œuf redevient fonctionnel
Dans leur article, les chercheurs ont travaillé sur une protéine du blanc d'œuf : le lysozyme. Le blanc d'œuf a été cuit pendant 20 minutes à 90 °C puis il a été dissous avec de l'urée pour retrouver une structure liquide. À cette étape, les protéines sont toujours inutilisables. C'est alors qu'intervient la deuxième étape : une centrifugation grâce à une machine puissante créée à la South Australia's Finders University.
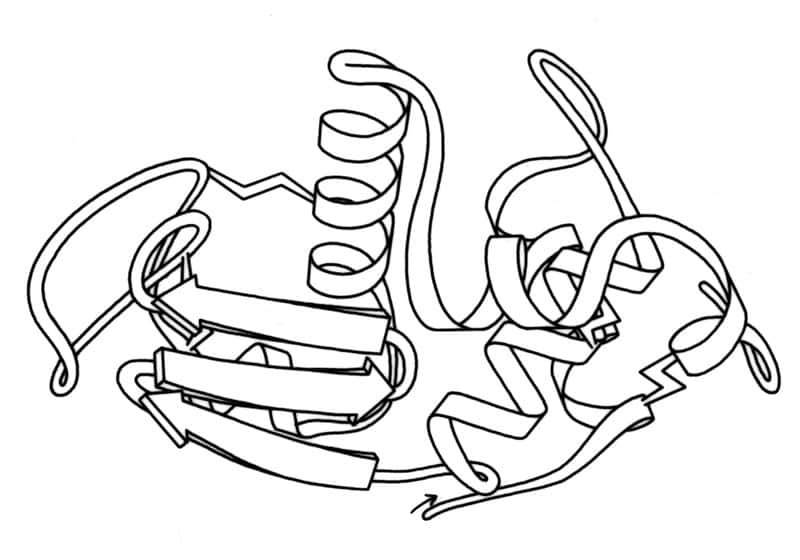
Le blanc d'œuf tourne dans un cylindre de verre de 10 mm par 16 cm à 5.000 tours par minute avec un angle de 45 °. Et alors miracle : le lysozyme a retrouvé son activité. Le procédé a aussi été utilisé avec de la cavéoline recombinante et une protéine plus grosse, la protéine kinasekinase A (ou cAMP-dependent protein kinase A : PKA).
C'est une victoire pour les chercheurs qui se sontlongtemps battus avec des protéines produites en laboratoire qui ne prenaient pas la forme voulue. Cette découverte pourrait apporter beaucoup à l'industrie pharmaceutique notamment.
Une révolution pour la production de protéines recombinantes
Cette méthode pourrait transformer la production de protéines pour la recherche et l'industrie. En effet, la production de protéines recombinantes est moins coûteuse dans des modèles comme la levure ou la bactériebactérie E. coliE. coli. Mais souvent les protéines produites n'ont pas la bonne configuration, forment des agrégats et ne se replient pas correctement. C'est pourquoi sont employés d'autres modèles cellulaires de production de protéines recombinantes, comme des cellules de mammifèresmammifères ou d'insectesinsectes -- des modèles bien plus coûteux. Par exemple, l'industrie pharmaceutique doit produire des anticorpsanticorps contre le cancercancer dans un modèle de cellules ovariennes de hamster, afin d'obtenir un bon repliement des protéines.
Il existe des méthodes pour récupérer du matériel mal replié, mais celles-ci sont chères et fastidieuses. L'équivalent d'une dialysedialyse à un niveau moléculaire nécessite plusieurs jours et des litres de liquide pour obtenir des mg de protéines. Le nouveau procédé décrit ici est bien plus rapide et économique. Il pourrait donc réduire les coûts de production de certains médicaments.