au sommaire
Des bactéries Escherichia coliEscherichia coli, appartenant au phylumphylum B2, contiennent un îlot génomique appelé PKS. C'est en s'intéressant à cet îlot génomique que des chercheurs de l'unité 1071 Inserm, Inra, université Clermont-Auvergne (Clermont-Ferrand) ont fait une découverte inattendue : ces E. coli empêchent la croissance de staphylocoques dorés multirésistants.
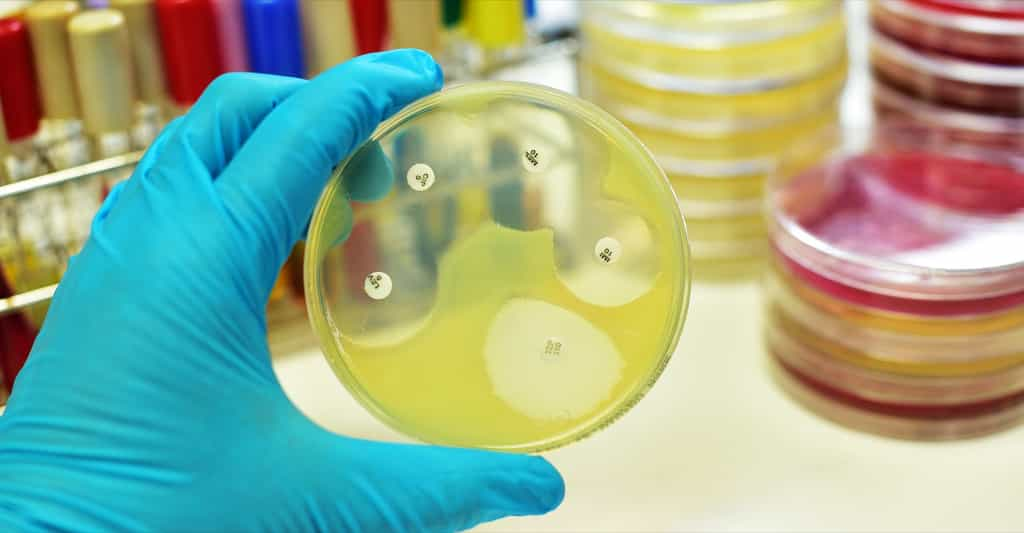
Cette propriété des bactéries E. coli porteuses de l'îlot PKS était bien visible lors de cultures sur boîte : si on les met au contact de S. aureus multirésistant, un anneau noir se forme autour de la colonie d'E. coli à cause de l'inhibition de la croissance. En revanche, autour de bactéries E. coli sans l'îlot PKS, la culture de staphylocoque reste uniforme.
Il reste donc à purifier les moléculesmolécules qui possèdent l'activité antibactérienne. Elles représentent un espoir pour traiter des infections multirésistantes aux antibiotiques.
----------
Article initial de Agnès Roux paru le 20/09/2013
Des chercheurs ont mis au point une stratégie pour caractériser l'action de nouveaux antibiotiques. Cette méthode devrait permettre de mieux cibler les médicaments, afin qu'ils soient plus performants et moins susceptibles d'engendrer des phénomènes de résistancerésistance.
Les antibiotiques sont des molécules fabriquées par des champignonschampignons ou des bactéries pour lutter contre les microbesmicrobes concurrents. On doit leur découverte à Alexander FlemingAlexander Fleming, à la fin des années 1920. L'histoire raconte que ce chercheur, bien que très doué, était par ailleurs assez désordonné et laissait souvent ses cultures bactériennes traîner un peu partout dans son laboratoire. Ce défaut lui aurait pourtant admirablement servi. En observant de près de vieilles boîtes de Petri, il se serait rendu compte que des champignons s'y étaient incrustés et empêchaient la croissance des bactéries. En analysant ce phénomène en détail, il montra que ces microbes envahisseurs produisaient une substance inhibitrice, qu'il appela pénicilline. Le premier antibiotique était identifié !
Cette découverte révolutionna la médecine infectieuse. À l'époque, la pénicillinepénicilline semblait être le remède miracle contre de nombreuses infections. Mais les bactéries avaient plus d'un tour dans leur sac. Peu de temps après les débuts de l'utilisation de la pénicilline, des germes résistants ont vu le jour. On sait maintenant que les microbes communiquent et s'échangent allégrement des gènesgènes, ce qui leur permet de mieux lutter contre les médicaments. Pour chaque nouvel antibiotique, ils réussissent à trouver rapidement une parade. La multirésistance aux antibiotiques est ainsi devenue un problème de santé publique majeur. Selon une étude récente du Center for Disease ControlCenter for Disease Control (CDC), les germesgermes super-résistants, ou « superbugs », tueraient 23.000 États-Uniens chaque année. Par comparaison, un peu plus de 15.000 personnes seraient mortes du SidaSida dans le pays en 2010 !

Alexander Fleming découvrit la pénicilline, un antibiotique sécrété par le champignon Penicillium notatum. Pour cette découverte, il a partagé le prix Nobel de physiologie ou médecine avec Howard Walter Florey et Ernst Boris Chain en 1945. © Wikimedia Commons, DP
Bientôt un antibiotique efficace contre le staphylocoque doré ?
Devant ce constat catastrophique, la mise au point de nouveaux médicaments antibactériens est primordiale. « Il n'existe plus d'antibiotique fiable, s'inquiète Joseph Pogliano, directeur de recherche à l'université de Californie à San Diego. De nouveaux antibiotiques arrivent régulièrement sur le marché, mais leur mode d'action n'est pas toujours connu ». Car pour savoir comment un antibiotique fonctionne, il faut parfois s'armer de patience. « Cela peut prendre plusieurs mois de travail intense », ajoute-t-il. Or, cette information est indispensable pour estimer l'efficacité d'un médicament. Pour pallier ce problème, Joseph Pogliano et son équipe ont développé une méthode rapide et efficace qui pourrait permettre de mieux cibler les médicaments antibactériens les plus performants. Cette étude est publiée dans la revue Pnas.
La technique, appelée profil cytologique bactérien, permet d'identifier les cibles bactériennes d'un nouvel antibiotique. Le principe est relativement simple. Les auteurs ont tout d'abord traité les bactéries avec cinq antibiotiques ayant chacun des modes d'action connus contre l'une des principales voies métaboliques de la cellule. En utilisant des techniques de coloration et de microscopie, ils ont pu montrer que chaque antibiotique modifiait la morphologiemorphologie et la structure des cellules bactériennes de manière spécifique. En réalisant la même expérience avec un antibiotique inconnu, il est ainsi possible d'estimer son mode d'action. « Il a fallu beaucoup de temps pour mettre la méthode au point, raconte Poochit Nonejuie, le principal auteur de ces travaux. Mais maintenant que nous la maîtrisons, il nous faut à peine une journée pour tester un nouvel antibiotique. »
Cette étude a permis la mise au point d'une stratégie ingénieuse pour l'identification de nouveaux antibiotiques. Reste maintenant aux chercheurs une lourde tâche : identifier la molécule magique qui permettrait de venir à bout des bactéries multirésistantes, comme le Sarm (Staphylococcus aureus résistant à la méticilline).