au sommaire

La maladie d'Alzheimer, développée par les personnes âgées, pourrait être traitée par des médicaments permettant l'activation de la protéine SIRT1. Crédits DR.
La maladie d'Alzheimer est la première cause de démence chez les personnes âgées, et touche actuellement 26 millions de personnes dans le monde. D'un point de vue biologique, elle est caractérisée par l'apparition et l'accumulation de plaques séniles, ou plaques amyloïdes dans le cerveau, qui perturbent son bon fonctionnement. Ces plaques sont composées de peptides beta-amyloïdes aussi appelés Aβ, qui proviennent de la dégradation des protéines APP (Amyloïd Protein Precursor) par la β-sécrétase. Un des moyens de lutter contre la maladie serait donc de réduire le clivageclivage.
Les chercheurs possèdent un modèle de la maladie chez la souris, où les symptômessymptômes et les causes moléculaires de la maladie sont équivalents à ceux retrouvés chez l'homme. Grâce à ce modèle murinmodèle murin, des chercheurs du Massachusetts Institute of Technology (MIT) ont voulu comprendre le lien entre une protéine impliquée dans le vieillissement, la protéine SIRT1, et la maladie d'Alzheimermaladie d'Alzheimer, elle-même due à l'âge.
En effet, la protéine SIRT1 appartient à la famille des « sirtuinessirtuines » qui régulent beaucoup de voies cellulaires, notamment celles impliquées dans le stress et dans la privation calorique. De plus, il y a 15 ans, les chercheurs avaient montré l'implication de la protéine sirtuine de levurelevure, nommée SIR2, dans la longévité cellulaire, et le rôle de la protéine avait été confirmé chez le ver, la souris et le rat.

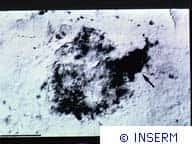
Les plaques amyloïdes, taches sombres révélées par un anticorps spécifique du peptide Aβ, sont plus nombreuses chez les souris modèles de la maladie exprimant la protéine SIRT1 à un taux normal (à gauche), que chez les souris surexprimant SIRT1 (à droite). © MIT / Cell
SIRT1 : 2 effets protecteurs
Dans un article du journal Cell, les chercheurs ont montré que la surexpression de la protéine SIRT1, chez les souris modèles de la maladie d'Alzheimer, inhibe l'apparition des plaques amyloïdes et ralentit la progression des symptômes de la maladie. A l'inverse, la mutation du gènegène sirt1 provoque la suraccumulation des plaques amyloïdes et l'aggravation des symptômes.
Les chercheurs ont analysé, au niveau moléculaire, le mécanisme impliquant SIRT1 dans la lutte contre la formation des plaques amyloïdes. La protéine SIRT1 possède des fonctions de déacétylase : elle a la capacité d'éliminer des modifications chimiques, de type acétyle, d'une autre protéine, nommée RARβ. En temps normal, RARβ inhibe l'expression de l'α-sécrétase. Lorsque RARβ est déacétylée par SIRT1, l'α-sécrétase peut être exprimée et cliver les protéines APP en des peptides différents de ceux formés par la β-sécrétase. Ainsi, plus l'α-sécrétase est active, moins la β-sécrétase a accès aux protéines APP pour former les peptides beta-amyloïdes pathogènespathogènes.
De plus, la surexpression de l'α-sécrétase grâce à SIRT1 permet aussi d'activer la voie de réparation des neuronesneurones endommagés : la voie Notch. La protéine SIRT1 a donc deux actions protectrices contre la maladie d'Alzheimer : la production compétitrice de peptides inoffensifs, et l'activation d'une voie cellulaire de protection des neurones.
Les scientifiques parlent déjà du développement potentiel de traitements thérapeutiques ou préventifs suite à cette découverte : des activateurs de la protéine SIRT1, impliqués dans la protection contre le vieillissement et la maladie d'Alzheimer, risquent de bientôt voir le jour.