Lorsqu'un récepteur ACE2 se fixe sur la protéine S qui entoure le coronavirus, celle-ci change de forme. Des scientifiques ont identifié dix structures, comme dix visages différents de la même protéine, qui permettent au virus d'infecter sa cellule-hôte.
au sommaire
La surface du SARS-CoV-2 est enveloppée par une membrane lipidique dans laquelle sont insérés des milliers de pics identiques connus sous le nom de spike protein ou protéine S. Cette protéine permet au virus d'entrer dans une cellule et d'y multiplier son génome.
Lors de la reconnaissance avec ACE2, son récepteur, la protéine S change plusieurs fois de structure tridimensionnelle pour permettre la fusionfusion des membranes cellulairesmembranes cellulaires et virales et initier l'infection. Une étude parue dans Nature et réalisée à l'Institut Francis-Crick a identifié dix formes différentes de la protéine S, de sa forme libre et sa forme finale.
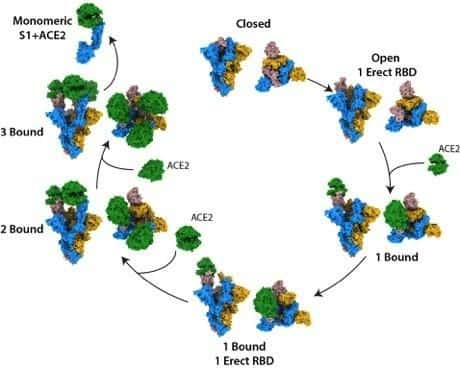
Dix structures différentes de la protéine S
Les scientifiques ont incubé un mélange contenant des protéines S du SARS-CoV-2 et des protéines ACE2. À différents stades, ils ont gelé rapidement dans l'éthane liquideliquide un fragment du mélange pour identifier les différentes formes du couple protéine S-ACE2. Les différentes structures qui se forment lors de la fixation d'ACE2 ont été déterminées par cryomicroscopie électroniquecryomicroscopie électronique.
Au début, la protéine S existe sous deux formes : ouverte et fermée. Dans la forme ouverte, le site de fixation de ACE2 est accessible ; dans sa forme fermée, il est caché. Lorsque ACE2 se fixe à un premier site de liaison, sur les trois disponibles, la protéine S s'ouvre un peu plus grâce à des changements de conformation. C'est sa troisième forme. À ce stade, deux autres ACE2 peuvent venir se fixer. Quand les trois sites de liaison sont pris, la partie centrale de la protéine est libre. La sous-unité S1 est déstabilisée et ses interactions avec la sous-unité S2 altérées. C'est cette forme qui permettrait l'infection en induisant les fusions des membranes. Au total, les scientifiques ont identifié dix structures différentes entre la première fixation d'ACE2 et la fusion des membranes.
« Nous pouvons voir que lorsque la protéine S devient plus ouverte, sa stabilité diminue, ce qui augmente sa capacité à réaliser la fusion des membranes, autorisant l'infection », explique Donald Benton, postdoctorant à l'Institut Francis-Crick, coauteur de cette recherche.
En comprenant les premières étapes de l'infection, les scientifiques espèrent découvrir de nouvelles cibles pour des antivirauxantiviraux déjà existants.