au sommaire
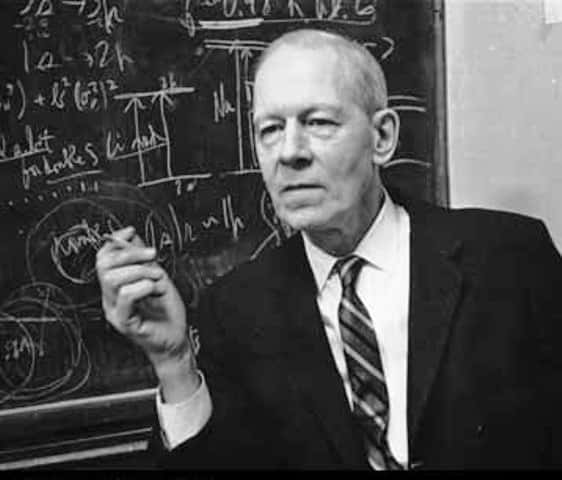
Robert Mulliken (1896-1986) est un physicien et chimiste américain principalement connu pour ses travaux sur le concept d'orbitale moléculaire et de la liaison chimique quantique. Il a obtenu le prix Nobel de chimie en 1966 pour ses travaux expliquant la structure des molécules. © AIP
En chimie quantique, le concept d'orbitale moléculaire repose sur la théorie de l'orbitale moléculaire (théorie OM ou théorie MO pour l'anglais molecular orbital)) développée à partir de la fin des années 1920 pour comprendre la formation et la structure des molécules dans le cadre de la théorie quantique. Construites à partir des orbitales atomiques des électrons de chaque atome constituant la molécule, les orbitales moléculaires décrivent donc les états électroniques au niveau des molécules.
Naissance de la théorie de l'orbitale moléculaire
Pour comprendre vraiment la formation des molécules, il a d'abord fallu attendre le début du XXe siècle pour que l'on perce les secrets de la liaison chimiqueliaison chimique. Ce n'est que lorsque Erwin SchrödingerErwin Schrödinger eut publié ses articles sur la mécanique ondulatoiremécanique ondulatoire, dans lesquels il exposait en 1926 la théorie de la célèbre équationéquation portant aujourd'hui son nom, que l'on a commencé à y voir plus clair. Quelques idées étaient cependant déjà posées. On savait que les forces électromagnétiques devaient jouer un rôle et, dès 1916, le chimiste américain Gilbert Lewis avait proposé le début de la théorie de la liaison covalenteliaison covalente entre atomes. Il s'agissait de la mise en commun d'électrons.
Mais il revint à Walter Heitler et Fritz London de donner, en 1927, la première explication quantique correcte de la liaison chimique, spécifiquement celle de la molécule de dihydrogène, à l'aide de l'équation de Schrödinger. Enfin, c'est principalement Robert Mulliken qui développa, avec d'autres, le concept d'orbitale moléculaire initialement introduit par Friedrich Hund.

De gauche à droite Robert Mulliken et Friedrich Hunden 1928 à Chicago. Le premier a développé le concept d'orbitale moléculaire quantique du second. ©
Les orbitales moléculaires de Hund et Mulliken
On sait, depuis la découverte du modèle de l'atome de Bohratome de Bohr, que les électrons se comportent comme s'ils étaient en orbiteorbite à des distances déterminées du noyau. Mais la comparaison s'arrête là. Les images montrant que l'atome est une sorte de mini-Système solaireSystème solaire en réduction sont trompeuses. Une représentation plus exacte serait celle d'un champ formant des concentrations particulièrement intenses, parfois en forme de coquilles, donnant les zones où il est possible de trouver, avec la plus grande probabilité, un électron autour d'un atome. Mais là aussi, ce n'est qu'une image grossière de la réalité physiquephysique, qui est plus ou moins associée à ce qu'on appelle techniquement une orbitale atomique pour un électron.
Ces champs autour des atomes peuvent se recouvrir l'un l'autre en s'additionnant ou se soustrayant à la façon de deux vaguesvagues entrant en collision à la surface de l'eau. Il se forme alors des orbitales moléculaires lorsque deux ou plusieurs atomes sont proches. Dans le premier cas, une énergieénergie de liaison apparaît entre les atomes, et l'on est en présence d'une liaison chimique. On parle alors d'orbitale liante. Dans le second cas, la soustraction produit une orbitale antiliante et une molécule ne peut pas se former.