au sommaire
Changement de phase à Lilliput
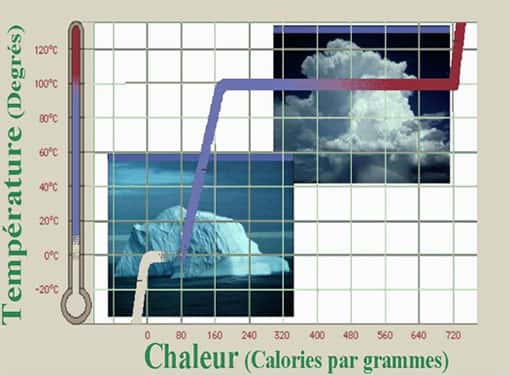
Quand on chauffe un liquide, on observe que sa température augmente jusqu'au moment où il est porté à ébullition. L'accroissement de température s'arrête alors miraculeusement, car toute la chaleur est utilisée pour transformer le liquide en vapeur. Cette propriété, très étrange si on y réfléchit, est bien utile pour la cuisson au bain-marie ! Vous êtes-vous jamais interrogé sur l'origine de ce curieux comportement ?
Depuis plusieurs années nous nous interrogeons sur l'origine physique de ces phénomènes si habituels et si dramatiques à la fois qui sont les transitions de phase. Nous recherchons une compréhension de ce qui se passe dans la matière, en l'observant à l'échelle microscopique de ses constituants élémentaires, atomes ou moléculesmolécules. Au cours de cette quête nous avons fait nombre d'étonnantes découvertes.

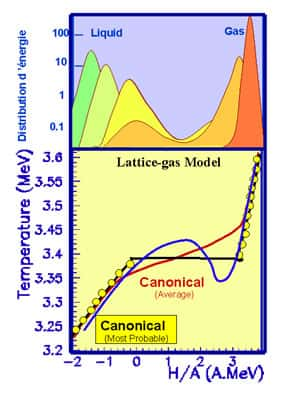
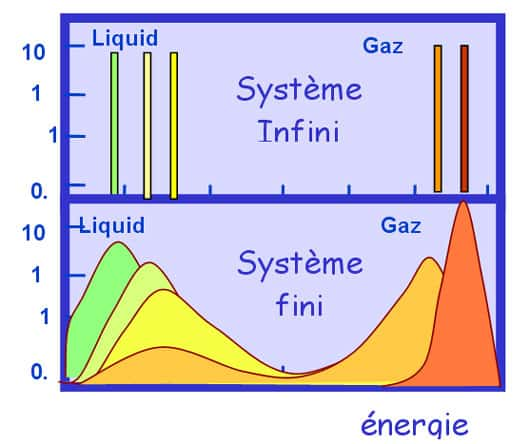
Quand on chauffe de la glace, les divers changements de phase sont caractérisés par des paliers de température. Si l'on ne contrôle pas l'énergieénergie fournie au système mais que l'on place celui-ci dans un four, ces paliers ne sont pas observables car si on est à peine en dessous de la transition, on se trouve à gauche du palier, alors que si on est juste au dessus de cette température on voit la partie droite. Il y a un saut brutal dans l'énergie du système. C'est la chaleur latente d'une transition du premier ordre.
A l'échelle des molécules, les lois de la thermodynamiquethermodynamique (et du bon sens commun) sont violées : il est possible de réchauffer un objet tout en lui pompant de la chaleur ! Encore plus surprenant, c'est justement ce comportement paradoxal qui permet d'expliquer pourquoi quand l'eau bout, c'est toujours à la même température, au millième de degré près !
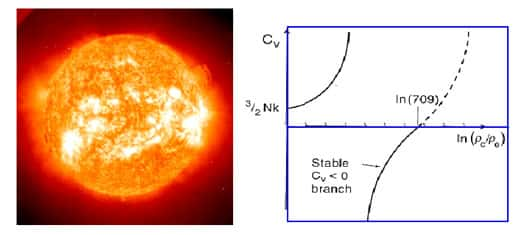
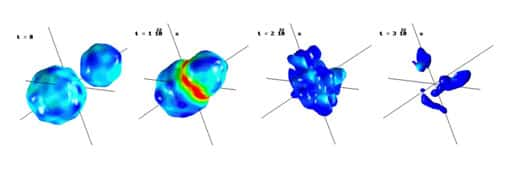
Au gré des découvertes, nous avons été surpris de voir que ce comportement contre-intuitif n'est pas spécifique du monde atomique et moléculaire, mais se retrouve à toutes les échelles : dans les étoilesétoiles et autres objets massifs de plusieurs centaines de milliers de kilomètres de rayon, jusqu'au cœur de l'atome, le noyau atomique, cet objet qui constitue toute la matière terrestre et est pourtant très difficile à imaginer, avec sa densité faramineuse de 250 millions de tonnes par centimètre cube et son diamètre un million de milliards de fois plus petit qu'un mètre.
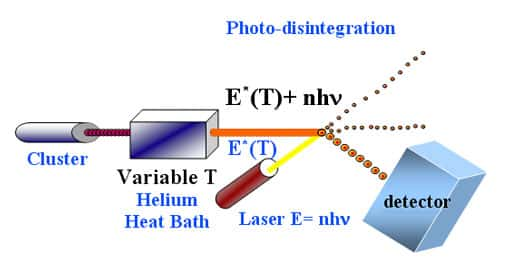
Eh bien quand ces objets, accélérés par nos accélérateurs de particules à des vitessesvitesses de l'ordre du tiers de la vitesse de la lumièrevitesse de la lumière, entrent en collision, ils se cassent en mille morceaux et dans cette cassure nous pensons avoir décelé à nouveau une émissionémission d'énergie thermiqueénergie thermique accompagnée d'un réchauffement du système de plusieurs milliards de degrés.
Venez avec moi à la découverte des paradoxes de l'infiniment petit et de son miroirmiroir, l'infiniment grand.