au sommaire
L'eau n'est pas la seule à avoir de telles propriétés : beaucoup d'autres molécules sont polaires comme elle. La vie extraterrestre a-t-elle vraiment besoin de l'eau liquide pour se développer ? Ne pourrait-elle pas trouver un autre liquide aux propriétés similaires ?

Ce serait oublier que l'eau est l'une des espècesespèces les plus communes dans l'Univers. Pour comprendre pourquoi, il suffit de noter l'abondance des différents éléments dans l'Univers :

L'abondance de l'hélium et de l'hydrogène est due au fait que ce sont les deux seuls éléments créés lors du Big Bang. L'oxygèneoxygène quant à lui est issu de la fusion nucléairefusion nucléaire qui a eu lieu dans les étoilesétoiles les plus massives, au même titre que tous les autres éléments.
Des candidats au remplacement de l'eau pour la vie ?
Parmi ces trois éléments, l'hélium est tout à fait inerte chimiquement. Il reste donc l'oxygène et l'hydrogène : les atomesatomes d'hydrogène peuvent ou bien se lier ensemble, formant H2 (la molécule la plus abondante dans l'Univers), ou bien se lier à un oxygène, formant H2O. Outre le dihydrogène, la molécule d'eau est donc la molécule la plus simple qu'on puisse former à partir des éléments les plus abondants de l’Univers... De toutes les molécules polaires, l'eau est de loin la plus courante.
Ainsi, l'eau est la molécule de la vie par excellence. Un coup d'œilœil sur la classification périodique vient renforcer cette conclusion : elle permet de mieux comprendre les propriétés chimiques exceptionnelles de cette molécule.
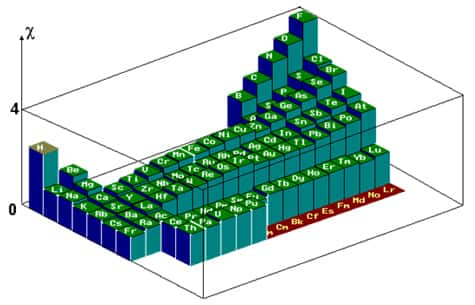
Si l'on exclut la dernière colonne, la capacité des atomes à attirer des électronsélectrons augmente d'en bas à gauche vers en haut à droite. On constate que le fluorfluor F est le « champion » dans ce domaine ; mais cet élément résout son besoin en captant un électron supplémentaire, formant ainsi l'ionion F-. Le fluor apparaît donc sous forme d'ions plutôt que sous forme de molécules.
Le deuxième élément qui tend le plus à attirer des électrons est l'oxygène. Cet élément voudrait former l'ion O2-, mais il n'en est pas capable car la formation d'une double charge négative sur un même atome est presque impossible (à cause de la répulsion électrostatiqueélectrostatique entre les deux charges négatives). C'est la raison pour laquelle l'oxygène tend à former des molécules plutôt que des ions. Son « besoin avide » en électrons attire vers lui les électrons d'une molécule : il se retrouve chargé négativement. C'est ce qui explique la polarité de la molécule d'eau, où l'oxygène porteporte une charge négative et les hydrogènes une charge positive.
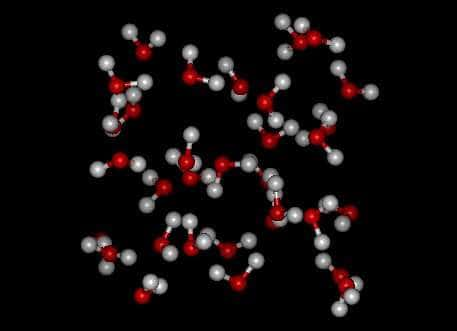
Finalement, de par cette propriété exceptionnelle de l'élément oxygène, l'eau H2O est la molécule la plus polaire qu'on puisse former parmi les espèces simples. Ses propriétés exceptionnelles de « collage » en font alors un fabuleux accélérateur de réactions.
Abondance exceptionnelle, propriétés chimiques exceptionnelles... L'eau est incontournable pour une vie extraterrestre hypothétique !