au sommaire
Comment les lymphocytes T sont-ils maintenus en repos ?
En quoi cette voie de la PI3-kinasekinase est-elle particulièrement importante pour l'amplification clonale ? Il faut introduire ici une notion importante, à savoir que l'état de repos d'une cellule n'est pas un état inactif. Il est en effet maintenu par la mise en œuvre de différents mécanismes moléculaires qui bloquent la cellule dans cette état, l'empêchant en particulier de se mette en cycle, le mot cycle (on parle en général de cycle cellulaire) désignant l'ensemble des étapes que doit franchir une cellule pour se diviser. Pour s'y engager un des moyens utilisés par la cellule est donc de lever ces freins permanents. Il s'agit de mécanismes absolument fondamentaux à l'œuvre dans beaucoup de types cellulaires et dont tout dérèglement peut avoir des conséquences dramatiques, puisqu'il conduit souvent à une prolifération anormale des cellules, synonyme de cancercancer.
La voie de la PI3-kinase contrôle l'un de ces freins représenté par les molécules de la famille FOXO (pour "forkhead box O protein"), et nos travaux ont permis de montrer que ces processus étaient effectivement impliqués dans la prolifération des LT déclenchée par la reconnaissance de l'antigèneantigène.

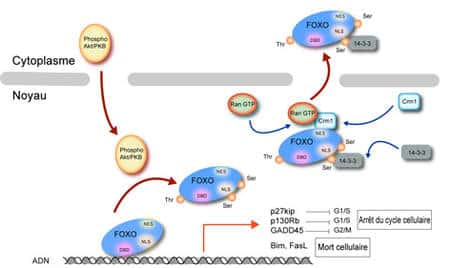
Légende : Les facteurs FOXO, majoritairement nucléaires dans les cellules au repos, sont des cibles de la kinase Akt qui les phosphoryle sur trois positions consensus (Thr14, Ser256 et Ser319 pour FOXO1). Cette phosphorylationphosphorylation permet l'association de FOXO avec la protéineprotéine 14-3-3 et sa prise en charge par une machinerie d'export nucléaire impliquant en particulier les protéines Ran et Crm1. Les FOXO, ainsi exclus du noyau, ne peuvent plus alors exercer leur activité transcriptionnelle. Ceci aura pour conséquences d'entraîner une baisse de production des ARN messagersARN messagers codant pour différentes protéines dont l'accumulation dans les cellules au repos bloque le cycle cellulaire (comme p27) ou favorise la mort cellulaire (comme Bim). Il est important de noter que la mutation des trois résidus cibles d'Akt en alaninesalanines inhibe l'export nucléaire des FOXO. Ces mutants constitutivement actifs ont été largement utilisés pour étudier les rôles fonctionnels de ces facteurs de transcriptiontranscription.
On peut tenter d'expliquer ce processus de manière assez simple (figure 11). Dans la cellule au repos, les FOXO sont dans le noyau où ils favorisent la régulation transcriptionnelle de nombreux gènesgènes, parmi lesquels on trouve des gènes codant pour de puissants inhibiteurs de la division cellulaire, comme la protéine p27. Ceci signifie qu'à l'état de repos de la cellule les FOXO sont actifs, cette activité ayant pour but de maintenir ces inhibiteurs à de hauts niveaux d'expression. Que se passe-t-il maintenant quand le LT est activé ? Une des conséquences en sera, nous l'avons-vu, l'activation de la PI3-kinase et plus en aval d'Akt. Or les FOXO sont des cibles privilégiées de cette dernière, ce qui entraînera leur phosphorylation par Akt.
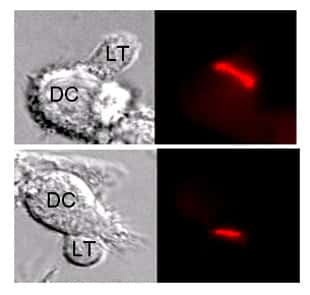
- Figure : 12
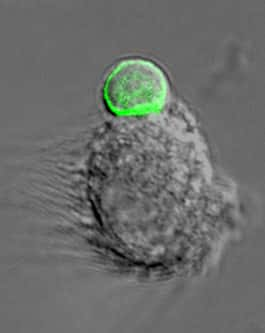
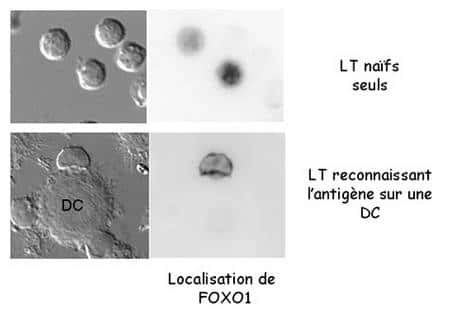
Légende : Images montrant la localisation de FOXO1, un des membres de la famille FOXO dans des LT naïfs non stimulées ou après leur interaction avec une DC présentant l'antigène. On voit clairement que la stimulationstimulation par l'antigène entraîne un changement majeur de cette localisation d'une position centrale, correspondant au noyau, vers la périphérie, correspondant au cytoplasmecytoplasme de la cellule.
Par des mécanismes complexes ceci provoquera l'exclusion des FOXO du noyau (voir la figure 12) et leur inactivation. Une baisse des niveaux d'expression des régulateurs négatifs du cycle cellulaire en résultera, conduisant à favoriser le démarrage de celui-ci.
Bien entendu beaucoup d'autres processus distincts et n'ayant rien à voir avec la voie de la PI3-kinase et les FOXO doivent être mis en jeu parallèlement. C'est vrai pour le LT comme pour la plupart des types cellulaires, soumis à des facteurs de croissancefacteurs de croissance par exemple. Il n'en reste pas moins vrai que cette voie est cruciale. La preuve en est que beaucoup de cancers humains sont liés à des mutations « activatrices » de la PI3-kinase ou à des accumulations anormales de PIP3 (par défaut de sa dégradation). Dans la plupart de ces cancers les FOXO sont donc inactivés ; mais il suffit de rétablir cette activité en introduisant dans les cellules tumorales des formes constitutivement actives de ces molécules (c'est à dire devenues insensibles à l'effet inhibiteur de la voie de la PI3-kinase) pour observer un arrêt spectaculaire de leur multiplication, puis leur mort. Ces différentes molécules (PI3-kinase, Akt, FOXO, etc.) sont donc aujourd'hui des cibles très prometteuses en chimiothérapiechimiothérapie anticancéreuse, au coeur de très nombreuses recherches pour identifier de petites molécules synthétiques qui seraient capables d'en modifier l'activité.