au sommaire
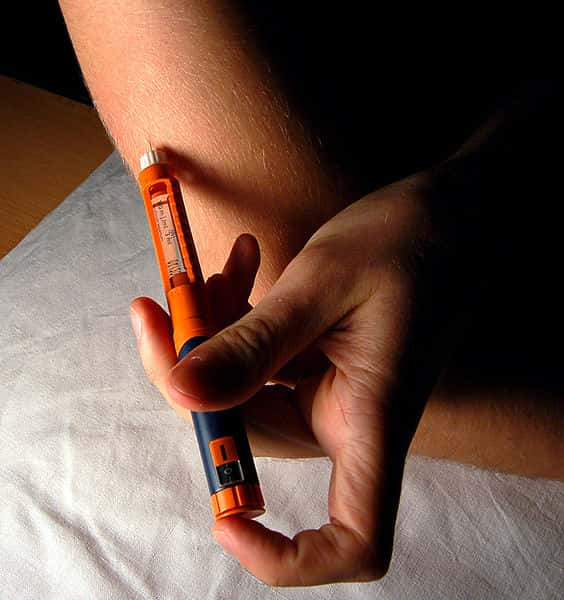
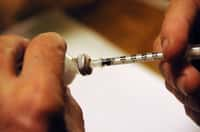
L'injection d'insuline est un acte quotidien pour des millions de diabétiques dans le monde. © Wikimedia Commons
Le diabète de type 1, ou insulinodépendant, est une maladie caractérisée par un défaut de synthèse de l'insuline. Cette hormone est habituellement produite par des cellules spécialisées du pancréas, les îlots de Langerhans (ou cellules β) et intervient dans la régulation de la glycémie. Elle favorise la conversion du glucose, moléculemolécule énergétique directement consommable, en glycogèneglycogène, un polymèrepolymère du glucose (forme de stockage).
Une glycémie trop élevée engendre des complications qui peuvent être graves et létales en quelques mois. Les diabétiquesdiabétiques de type 1 doivent donc lutter quotidiennement contre l'hyperglycémie en s'injectant plusieurs fois par jour de l'insuline. Ce n'est donc pas un traitement curatifcuratif puisque la cause elle-même de la maladie n'est pas soignée.
Les avancées de la thérapie cellulaire
La thérapie cellulairethérapie cellulaire s'avère être une solution d'avenir, car elle permettrait de rétablir la synthèse de l'insuline par l'organisme. Des essais de thérapie cellulaire publiés en 2009 avaient d'ailleurs déjà montré leur efficacité sur plusieurs patients. Les cellules de donneurs réimplantées dans le foie des malades permettaient à 57% d'entre eux de vivre sans les injections quotidiennes d'insuline.
Les chercheurs de l'unité Inserm 859 "Biothérapies du diabètediabète" dirigée par François Pattou (Université de Lille-Nord de France, CHRU de Lille) ont réalisé une nouvelle avancée en thérapie cellulaire, en réalisant une autogreffeautogreffe de cellules β sur une patiente au profil particulier. Cette femme, victime d'une tumeurtumeur du pancréas (insulinome) s'était vue retirer plus de 80% de son pancréas. La diminution du nombre total de cellules produisant l'insuline aurait dû favoriser l'apparition d'un diabète de type 1 et elle en montrait d'ailleurs les premiers signes juste après l'opération.
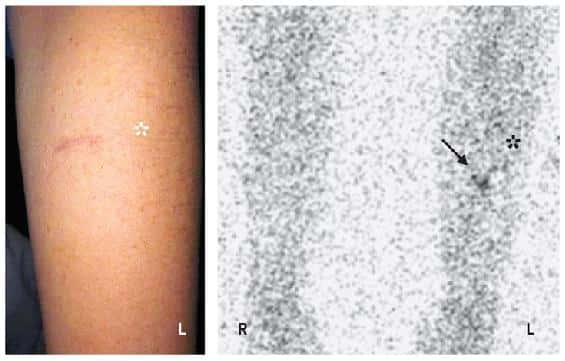
L'image de gauche correspond à la photographie du bras gauche de la patiente. L'image de droite correspond à l'observation des deux bras (R = bras droit ; L = bras gauche) de la patiente par scintigraphie. La flèche indique la position du marquage et donc des cellules β. L'étoile indique la position de la cicatrice laissée par l'implantation des cellules. © NEJM
53 % d'insuline sécrétée par les cellules réimplantées
Pour éviter le développement du diabète, et pour éviter toute complication due à la tumeur, les chercheurs ont décidé de réimplanter ses propres cellules du pancréas retiré (saines et sécrétrice d'insuline) non pas dans le foiefoie mais dans le muscle de l'avant-bras (le muscle brachio-radial).
Un an après l'injection des cellules β, la régulation de la glycémie de la patiente semble être efficace, d'après les résultats publiés dans le journal The New England Journal of Medicine. Pour vérifier la provenance de l'insuline (des cellules du pancréas restantes ou des cellules réimplantées), le taux d'insuline a été mesuré dans les deux bras, après l'injection d'argininearginine (qui stimule aussi la production d'insuline).
Un pic est observé dans le bras gauche qui contient les cellules β, et une plus légère augmentation est perçue dans le bras droit (13,1 milliunités par litre). Si la circulation sanguine est coupée au niveau du bras gauche (l'insuline produite par les cellules réimplantées ne sera pas diffusée), l'augmentation du taux d'insuline dans le bras droit est plus faible (6,1 milliunités par litre). Les cellules β situées dans le bras gauche sont donc responsables de 53% de la production totale d'insuline.
En plus de cette réussite, les chercheurs ont pu mettre au point une méthode de détection des cellules β de sécrétionsécrétion de l'insuline par une méthode non invasive. Ils ont utilisé un marqueur du récepteur du GlucagonGlucagon-like peptide 1 (une protéineprotéine très exprimée dans ces cellules) pour révéler spécifiquement les cellules β par scintigraphiescintigraphie. Si le bruit de fond est similaire dans les deux bras, une tache plus dense indique la présence de cellules β juste à coté de la cicatricecicatrice laissée par l'intervention.
Ces résultats montrent que les cellules β sont capables de survivre et de fonctionner dans un autre contexte. En attendant l'utilisation (peut-être) à grande échelle du pancréas artificiel présenté en avril, ces travaux améliorent les connaissances sur la thérapie cellulaire et permettent d'envisager de nouveaux traitements contre le diabète ou contre d'autres maladies.