au sommaire
Les quatre décès font les gros titres mais cette aventure est pour l'heure un succès. La réussite du protocoleprotocole était en effet évaluée selon le taux de survie à 30 jours de patients insuffisants cardiaques, tous sévèrement atteints. Le premier a vécu 74 jours, le deuxième neuf mois et le troisième huit mois. Quant au quatrième, il est décédé 26 jours après l'implantation.
Dans son ensemble, « le système cumule une expérience clinique de 21 mois de fonctionnement » (dixit CarmatCarmat) cependant l'ANSM (l'Agence nationale de sécurité du médicament et des produits de santé) peut demander à la société française de réaliser une nouvelle implantation afin d'obtenir un quatrième patient à au moins 30 jours de survie (et non 26), comme le prévoient les critères fixés dans l'étude de faisabilité. Avec ce dernier patient, l'équipe française semble avoir pris un risque, motivé par son jeune âge (58 ans). Il souffrait en effet, avant l'intervention, d'une « défaillance bi-ventriculaire sévère dont l'évolution avait nécessité la mise sous assistance circulatoire extracorporelle (ECLS) », est-il expliqué dans le communiqué de presse.
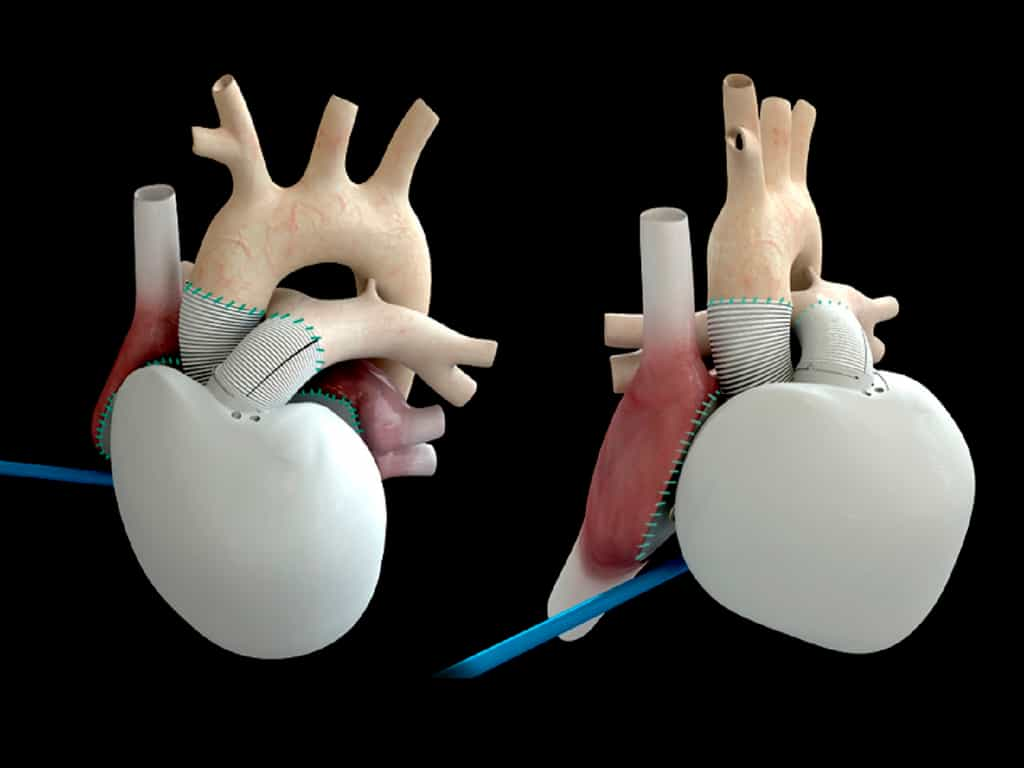
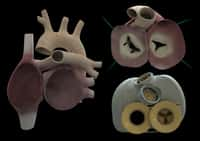
L'équipe médicale, comme les représentants de la société apparaissent toutefois confiants pour entamer la prochaine phase, à savoir une étude de phase III. Elle devrait être réalisée dans les mois qui viennent auprès de 20 à 50 patients, dans plusieurs pays européens. La France, donc, mais aussi l'Allemagne, l'Autriche, l'Espagne et encore l'Italie. Au cours des prochaines semaines, des équipes médicales seront d'ailleurs formées à cette intervention. L'enjeu est de taille. Il s'agit d'aboutir au marquage CE. Lequel ouvrira la porteporte à une commercialisation de ce cœur artificiel total, qui, rappelons-le, n'est pas un greffon sujet à rejet, comme les études exposées dans la vidéo qui suit cet article.