au sommaire
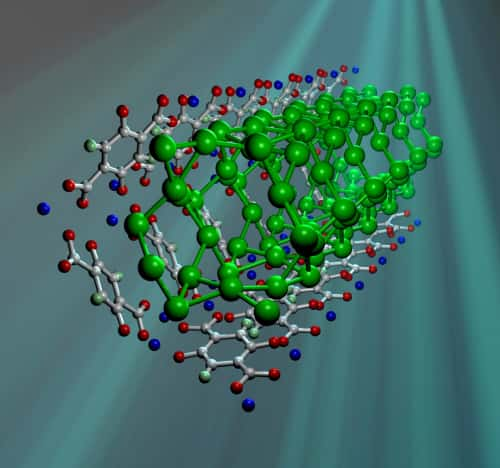
Figure 1. Molécules d'hydrogène (vert) stockées dans du MOF-74. Crédit : NIST
Introduits par Omar Yaghi il y a quelques années, les MOF (Metal-Organic Frameworks) font partie des matériaux les plus sérieusement étudiés pour produire un jour des dispositifs pratiques et efficaces pour stocker de l'hydrogène et remplacer l'essence dans les voituresvoitures. Très poreux, ces matériaux renferment au sein d'un réseau cristallinréseau cristallin un grand nombre de cavités nanométriques, qui les font ressembler au zéolithe naturel. Ce volume intérieur peut retenir des gaz, et en particulier l'hydrogène.
En effet, pour stocker suffisamment d'hydrogène dans un faible volume et permettre de concurrencer les moteurs à essence, on ne dispose aujourd'hui que, peu ou prou, de deux solutions : le refroidir pour le liquéfier à quelques degrés au-dessus du zéro absolu ou le comprimer sous des pressionspressions élevées.
D'après les chercheurs du National Institute of Standards and Technology's Center for NeutronNeutron Research (NCNR, Etats-Unis), les études sur la structure du MOF 74 menées à l'aide de la diffusiondiffusion de neutrons ainsi que les expériences d'adsorptionadsorption ont montré que ce matériaumatériau pouvait absorber plus d'hydrogène que tous les autres en l'absence de pression, et surtout, à une température de seulement 77 K (kelvinskelvins). Mieux, il n'y a pas besoin de le porter à des températures de 110 à 500 °C pour provoquer la libération de l'hydrogène stocké, comme c'est le cas avec les autres matériaux.
700 mètres carrés par gramme
Les chercheurs ne comprennent pas encore très bien d'où le MOF 74 tire ses étonnantes propriétés. Ils savent bien sûr qu'ils sont en présence d'une poudre cristalline très poreuse et composée d'atomesatomes de carbonecarbone (en blanc sur la figure 1) et de zinczinc (en bleu) et formant une série de paillettes. La nanoporosité est telle qu'un gramme de cette poudre possède une surface effective de deux terrains de basket-ball, soit plus de 700 mètres carrés. Ce serait au niveau des atomes de zinc dans cette structure que l'interaction avec l'hydrogène serait particulière.
S'ils ont raison, et que l'on pouvait comprendre vraiment son effet sur l'augmentation de la densité de stockage de l'hydrogène à - relativement - haute température, on pourrait peut-être enfin concevoir des matériaux ayant les bonnes capacités de stockage, et surtout, fonctionnant à une température proche de la température ambiante.