Une molécule ionisée formée à partir de l'hélium, HeH+, suggérait une solution à l'énigme de la formation des premières étoiles. On vient de montrer que cette molécule pouvait effectivement se former dans des conditions similaires à celles régnant au moment où les premiers atomes neutres ont commencé à naître, 380.000 ans après le début du cosmos observable. Cette molécule pourrait même avoir été la première à se former à ce moment-là.
au sommaire
AstrophysiciensAstrophysiciens et cosmologistes sont confrontés depuis longtemps à une énigme lorsqu'ils veulent comprendre la formation des premières étoiles. Pour comprendre de quoi il en retourne, il faut se rappeler quelques éléments de la théorie générale de la formation des étoiles. Lorsqu'on expose cette dernière, on commence par introduire le célèbre critère de Jeans, lequel montre que dans certaines conditions de densités et de températures il existe une masse limite pour un nuagenuage de gaz au-dessus de laquelle il doit s'effondrer, puis se fragmenter, pour donner des étoiles sous l'effet de sa propre gravité.
Des nuages moléculaires pouponnières d'étoiles
Mais à y regarder de plus près, ce processus ne va pas de soi. La première complication est celle de la conservation du moment cinétique. Il implique qu'un nuage en rotation en train de s'effondrer voit sa vitessevitesse angulaire augmenter, à la façon d'une patineuse qui rapproche ses bras. Il en résulte que les forces centrifugesforces centrifuges augmentent et peuvent arrêter l'effondrementeffondrement du nuage dans son plan équatorial. Or, les nuages moléculaires qui servent de pouponnières d'étoiles sont tous un peu turbulents, ce qui veut dire que la fragmentation va produire des poches de matièrematière en rotation.
En outre, s'il y règne un champ magnétiquechamp magnétique, la conservation du flux magnétique fait augmenter la pressionpression magnétique à l'intérieur du nuage en contraction, ce qui, là aussi, menace d'empêcher sa contraction.
Enfin et surtout, cette contraction augmente la température du nuage de gaz, ce qui fait grimper sa pression, conduisant également à bloquer l'effondrement gravitationnel et empêcher la formation d'une étoile.
Ce dernier problème est résolu par la Nature grâce à la présence dans les nuages moléculaires de poussières et de moléculesmolécules de CO et même d'H2O. En s'échauffant, les poussières et ces molécules rayonnent de l'énergieénergie dans l'infrarougeinfrarouge, permettant au nuage de se refroidir et par là même de continuer sa contraction pour donner une protoétoileprotoétoile.
Malheureusement, ce problème resurgit pour la formation des premières étoiles, celles dites de population IIIpopulation III, pendant les Âges sombresÂges sombres au cours des premiers millions d'années de l'histoire du cosmoscosmos observable.
En effet, la nucléosynthèsenucléosynthèse primordiale n'a pas produit les éléments lourds que sont le carbonecarbone et l'oxygèneoxygène que l'on trouve dans les poussières et les molécules CO. Or, comme on vient de le voir, sans eux, pas d'étoiles. Pourtant, ces éléments ne seront synthétisés que plus tard, précisément dans les étoiles massives. On est donc confronté au dilemme de l'œuf et de la poule.
Une présentation de l'importance de la découverte de l’ion HeH+ dans l'espace. Pour obtenir une traduction en français assez fidèle, cliquez sur le rectangle blanc en bas à droite. Les sous-titres en anglais devraient alors apparaître. Cliquez ensuite sur l'écrou à droite du rectangle, puis sur « Sous-titres » et enfin sur « Traduire automatiquement ». Choisissez « Français ». © Nasa's Ames Research Center
HeH+ et H2 : des clés de l'énigme de la naissance des premières étoiles ?
Il existe pourtant au moins une solution, proposée dès 1967 par Saslaw et Zipoy. Elle fait intervenir une autre molécule dont on sait qu'elle joue aussi le rôle d'un radiateurradiateur lors de la formation stellaire, la molécule H2. L'incertitude porteporte sur la quantité de molécules d'hydrogènehydrogène qui pouvait apparaître à cette époque. C'est pourquoi on étudie les phénomènes qui pourraient conduire à une formation précoce et importante d'hydrogène moléculaire juste au moins au moment où sont en train d'apparaître les premiers atomesatomes.
Une des théories proposées à ce sujet vient d'être confortée par une découverte faite par une équipe internationale d'astrophysiciens menée par Rolf Güsten de l'Institut Max-PlanckPlanck pour la radioastronomie (MPIfR) à Bonn, en Allemagne. Elle est exposée dans un article publié dans le prestigieux journal Nature et elle concerne la première détection dans l'espace interstellaire d'une molécule baroque que l'on pourrait croire impossible, l'hydrure d'héliumhélium HeH+.
L'hélium est un gaz rare, à première vue chimiquement inerte et incapable de former des molécules. En fait, ce n'est pas toujours le cas, dès 1925 on avait fait la découverte de l'ionion HeH+ en laboratoire. Dans les années 1970, les astrochimistes se sont rendu compte que cette molécule devait pouvoir se former au moins dans le milieu interstellaire quand des conditions favorables étaient réunies. On avait cherché jusqu'ici, en vain, sa trace mais tout vient de changer grâce à des observations faites dans l'infrarouge lointain avec un instrument à bord de Sofia (Stratospheric Observatory for Infrared AstronomyStratospheric Observatory for Infrared Astronomy), un avion montant dans les couches hautes de l'atmosphèreatmosphère pour faire des observations en infrarouge qui ne sont pas possibles au sol du fait de la présence de trop grandes quantités de vapeur d'eau dans l'atmosphère basse.
Sofia a donc finalement permis de découvrir la signature des molécules HeH+ dans une nébuleuse planétaire, NGCNGC 7027, située à environ 3.000 années-lumièreannées-lumière du Système solaireSystème solaire dans la constellationconstellation du Cygne. Âgée d'environ 600 ans, c'est le produit d'une étoile devenue une naine blanchenaine blanche et dont le rayonnement intense provoque la synthèse de l'hydrure d'hélium en ionisant des atomes.
HeH+ 380.000 ans après le Big Bang ?
HeH+peut donc bien naître dans des conditions astrophysiquesastrophysiques particulières qui ressemblent à celles qui existaient environ 380.000 ans après le début de l'UniversUnivers observable, au moment où son contenu se refroidissait suffisamment pour commencer à former les premiers atomes neutres, en l'occurrence essentiellement d'hydrogène et d'hélium puisqu'il n'existait pas alors de noyaux plus lourds que le lithiumlithium.
En fait, on pense qu'avec leurs potentiels d'ionisationionisation plus élevés, les ions hélium He2+ et He+ ont été les premiers à se combiner avec les électronsélectrons libres du plasma primordial juste avant l'émissionémission du fameux rayonnement fossile, formant ainsi les premiers atomes neutres avant ceux d'hydrogène. Les ions H+, qui existaient encore, pouvaient donc se combiner avec les atomes neutres d'hélium et les premières molécules du cosmos observable auraient même été celles de HeH+.
On a donc maintenant des raisons supplémentaires de penser que les réactions menant à la formation précoce d'hydrogène moléculaire grâce à l'ion HeH+ pouvaient bien avoir eu lieu au début de l'histoire de l'Univers et qu'elles ont contribué à la naissance des premières étoiles, selon une étape importante de l'évolution menant du Big Bang au vivant.
Des molécules d'hélium "impossibles" autour des naines blanches ?
Article de Laurent SaccoLaurent Sacco publié le 25/07/2012
La formation de molécules d'hélium sur Terre reste très difficile et l'on a même longtemps pensé qu'elle était impossible. D'après des simulations sur ordinateurordinateur, tout changerait dans le cas d'atomes d'hélium plongés dans les champs magnétiques intenses des naines blanches et des étoiles à neutronsétoiles à neutrons.
Il a fallu attendre le début du XXe siècle pour percer les secrets de la liaison chimiqueliaison chimique. Ce n'est que lorsque Erwin SchrödingerErwin Schrödinger eut publié ses articles sur la mécanique ondulatoiremécanique ondulatoire, dans lesquels il exposait en 1926 la théorie de la célèbre équationéquation portant aujourd'hui son nom, que l'on a commencé à y voir plus clair. Quelques idées étaient cependant déjà posées. On savait que les forces électromagnétiques devaient jouer un rôle et, dès 1916, le chimiste américain Gilbert Lewis avait proposé le début de la théorie de la liaison covalenteliaison covalente entre atomes. Il s'agissait de la mise en commun d'électrons.
Mais il revint à Walter Heitler et Fritz London de donner, en 1927, la première explication quantique correcte de la liaison chimique, spécifiquement celle de la molécule de dihydrogène, à l'aide de l'équation de Schrödinger. Enfin, c'est principalement Robert Mulliken qui développa, avec d'autres, le concept d'orbitale moléculaireorbitale moléculaire (modèle décrivant les états électroniques de molécules) bien connu des chimistes quantiques de nos jours.
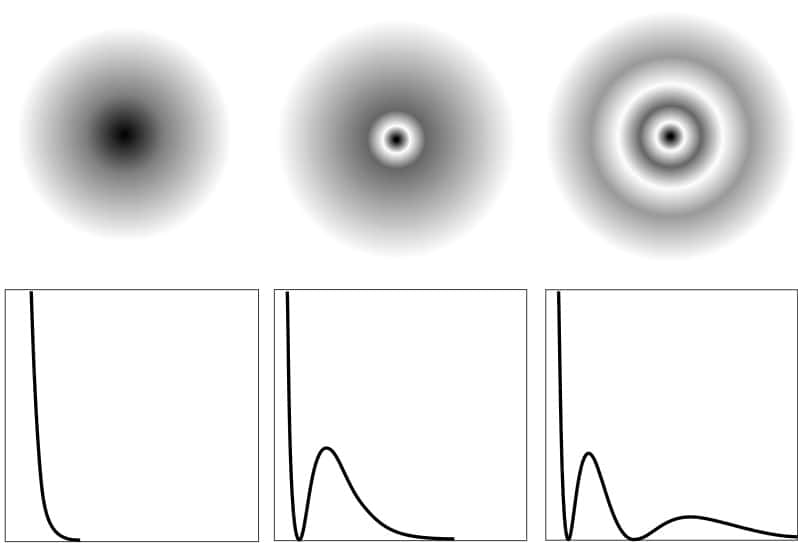
On sait, depuis la découverte du modèle de l'atome de Bohratome de Bohr, que les électrons se comportent comme s'ils étaient en orbiteorbite à des distances déterminées du noyau. Mais la comparaison s'arrête là. Les images montrant que l'atome est une sorte de mini-Système solaire en réduction sont trompeuses. Une représentation plus exacte serait celle d'un champ formant des concentrations particulièrement intenses, parfois en forme de coquilles, donnant les zones où il est possible de trouver, avec la plus grande probabilité, un électron autour d'un atome. Mais là aussi, ce n'est qu'une image grossière de la réalité physiquephysique, qui est plus ou moins associée à ce qu'on appelle techniquement une orbitale atomique pour un électron.
Ces champs autour des atomes peuvent se recouvrir l'un l'autre en s'additionnant ou se soustrayant à la façon de deux vaguesvagues entrant en collision à la surface de l'eau. Il se forme alors des orbitales moléculaires lorsque deux ou plusieurs atomes sont proches. Dans le premier cas, une énergie de liaison apparaît entre les atomes, et l'on est en présence d'une liaison chimique. On parle alors d'orbitale liante. Dans le second cas, la soustraction produit une orbitale antiliante et une molécule ne peut pas se former.
Une nouvelle liaison chimique grâce au champ magnétique
Appliquer la théorie aux atomes d'un gaz rare, l'hélium, semble tout d'abord conduire à l'impossibilité de la formation d'une molécule diatomique d'hélium. Comme on l'a découvert par la suite, il existe des situations dans lesquelles des molécules d'hélium, bien que faiblement liées et instables, peuvent se former. On connaît ainsi le cas des molécules d'hélium exotiquesexotiques ultrafroides.
Mais selon des chercheurs qui viennent de publier un article dans Science, il serait possible d'obtenir, à partir des orbitales antiliantes, une molécule d'hélium stable dans certaines situations.
En employant un programme baptisé London, visiblement en référence à Fritz London, ils ont découvert que tout changerait si des atomes d'hélium étaient placés dans un champ magnétique particulièrement intense d'au moins 105 teslasteslas (sur Terre, les champs magnétiques les plus intenses produits en laboratoire atteignent 30 à 40 teslas, T). Un nouveau type de liaison chimique stable deviendrait donc possible.
Il s'agit de spéculations purement théoriques mais, en tout état de cause, des champs aussi intenses se trouvent à la surface des étoiles à neutrons et des naines blanches. Il existe donc, peut-être, des molécules à la chimiechimie exotique à bonne distance de ces astresastres (car il faut qu'elles ne soient pas détruites aussitôt formées par les rayonnements émis par les étoiles). Il faudrait, tout de même, que le champ magnétique y soit encore suffisamment intense.

Ce qu’il faut
retenir
- L'hélium est généralement inerte chimiquement mais il peut parfois former des molécules comme l'ion HeH+ que l'on a déjà détecté en laboratoire en 1925.
- On cherchait depuis longtemps la présence de cet ion dans le milieu interstellaire, car non seulement il devait y apparaître mais sa présence dans l'Univers primordial après l'émission du rayonnement fossile pouvait résoudre une énigme importante.
- Des poussières et des molécules carbonées permettent la naissance des étoiles de nos jours ; or, les atomes de carbone n'ont pas été produits par le Big Bang mais dans les étoiles. On a donc du mal à comprendre comment sont nées les premières étoiles.
- On peut résoudre l'énigme en faisant intervenir de l'hydrogène moléculaire mais encore faut-il en former juste après le Big Bang.
- C'est possible notamment avec l'ion HeH+ qui aurait même été la première molécule existante, environ 380.000 ans après le Big Bang.
- On vient de détecter cette molécule dans une nébuleuse planétaire ce qui nous assure que ces molécules pouvaient bien apparaître précocement.