au sommaire
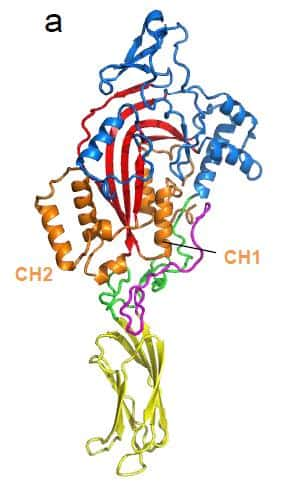
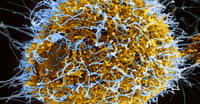
La perforine, produite par des lymphocytes, crée des pores à la surface des cellules dangereuses pour l'organisme. Sa structure a été élucidée aux rayons X. © Nature
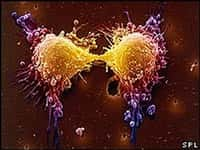
Les cellules immunitaires utilisent diverses tactiques pour protéger l'organisme contre les agressions. Après près de 10 ans de recherche, des scientifiques australiens et britanniques ont enfin décrypté le mécanisme d'action d'une protéine impliquée dans un mécanisme essentiel à l'immunité : la perforine.
Elle est contenue dans des granules cytoplasmiques de cellules immunitaires particulières : les lymphocytes NK (natural killer) et les lymphocytes T cytotoxiquescytotoxiques. Lorsque ces vigiles rencontrent une cellule dangereuse (cancéreuse ou infectée par un virus), une « synapse immunitaire » est créée, menant à l'activation d'un mécanisme de défense particulier.
Perforation de la membrane
En premier lieu, la perforine est larguée du lymphocyte vers la cellule cible. S'assemblant avec d'autres perforines, elles créent une sorte de pore transmembranaire dans la membrane de la cellule cible. La perforine porteporte donc bien son nom puisqu'elle est effectivement capable de perforer les cellules à éliminer.
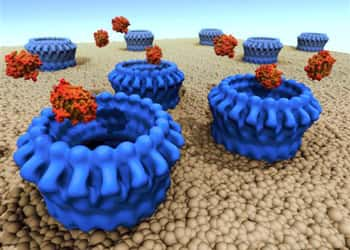
Plusieurs perforines s'assemblent pour former des pores dans les membranes des cellules à éliminer. © Monash university
Ensuite, des protéasesprotéases du nom de granzymesgranzymes sont aussi larguées vers la cellule cible et passent à travers les pores formés par les perforines. Une fois dans le cytoplasmecytoplasme de la cellule cible, les granzymes dégradent progressivement le contenu de la cellule, activant ou désactivant divers processus menant finalement à une mort par apoptose.
La perforine est absolument essentielle au mécanisme de défense assuré par les lymphocytes T cytotoxiques, alors que la redondance des différents types de granzymes permet un remplacement éventuel d'une enzymeenzyme par une autre. Des études menées sur les souris avaient d'ailleurs montré qu'une déficience en perforine menait à une suraccumulation de cellules cancéreuses, en particulier des leucémiesleucémies. Chez l'homme, une grande partie des cas de lymphohistiocytoses hémophagocytaires, des maladies immunitaires sévères, sont liées à une mutation dans le gènegène de la perforine.
Structure proche des pores bactériens
Pourtant, le mode d'action de la perforine était encore mal connu avant la publication récente d'un nouvel article dans la prestigieuse revue Nature. Il a finalement pu être élucidé grâce à l'utilisation d'imageries moléculaires puissantes. Les chercheurs ont déterminé, grâce aux rayons Xrayons X, la structure de la perforine monomérique de souris. Ils ont également obtenu une image par cryo-microscopie électronique (après congélation de l'échantillon) d'un pore entier (perforine multimérique).
Les images obtenues permettent d'observer que la perforine est une protéine en forme de clé, composée de plusieurs domaines et que la fixation à la membrane nécessite la présence d'ionsions calciumcalcium. De manière plus surprenante, la microscopie électronique a révélé que l'arrangement des perforines ressemble à celui des protéines bactériennes toxiques pour les cellules humaines (anthrax, listéria, streptocoque...).
Ces travaux finalisent ce que Jules Bordet, prix Nobel de médecine et de physiologie en 1919, avait découvert il y a 110 ans. « Maintenant que l'on sait comment cela fonctionne, on peut commencer à l'affiner pour combattre le cancercancer, le paludismepaludisme et le diabètediabète » affirme James Whisstock de l'université Monash, le principal auteur de l'article.