au sommaire
Grâce à six semaines de travail, des centaines d'auditions et l'analyse de documents s'échelonnant sur 40 ans, l'Inspection générale des affaires sociales (Igas) a pu déterminer la chronologie des événements et identifier les responsables du scandale du Mediator qui a fait au moins 500 morts. Retiré en 2009, le médicament, aujourd'hui accusé pour son inefficacité et sa dangerosité, aurait provoqué des valvulopathies chez un grand nombre de patients sous traitement.
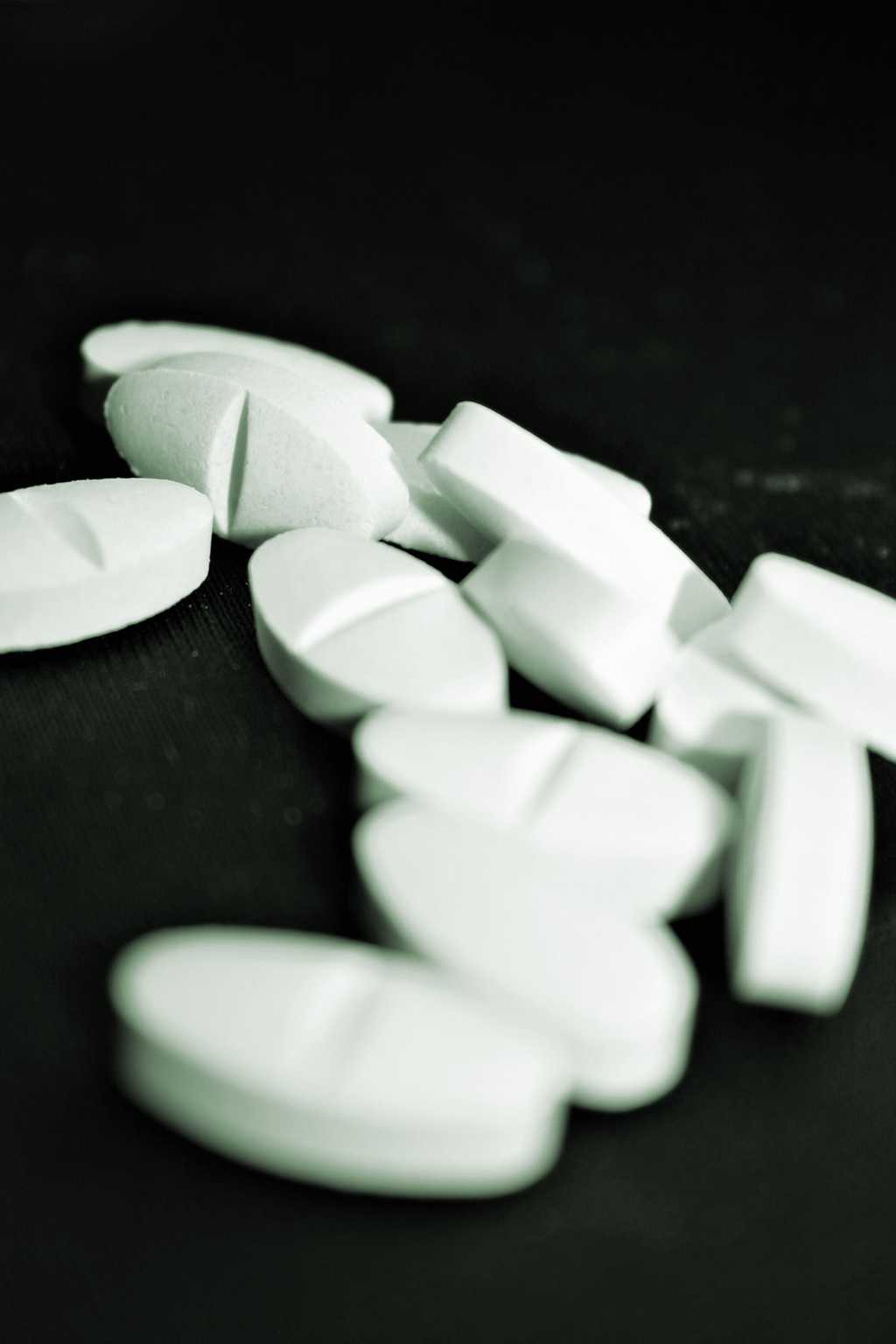
Mais revenons sur les faits. Dans les années 1960, le laboratoire Servier cherchait à obtenir des moléculesmolécules coupe-faim dépourvues d'effets indésirables, dérivées des amphétamines qui possèdent naturellement cette propriété mais dont les effets secondaires sont lourds. Les recherches ont mené à l'obtention de deux molécules, la fenfluramine, qui sera effectivement commercialisée comme coupe-faim sous le nom de Ponderal en 1963, et le benfluorex, mieux connu sous le nom de Mediator, commercialisé en 1976 comme antidiabétique, celui-là.
Un coupe-faim...
Or ces deux molécules possèdent un point commun indiscutable : elles se métabolisent dans l'organisme sous forme de norfenfluramine, une amphétamine modifiée (ajout d'un groupement trifluoré) qui possède toujours la propriété coupe-faim, selon des études effectuées au début des années 1960.
D'après le rapport de l’IGAS, « les trois molécules en question - norfenfluramine, fenfluramine et benfluorex - sont pharmacologiquement, méthodologiquement et chronologiquement liées », et leur propriété pharmacologique repose donc principalement sur l'action anorexigène de la norfenfluramine.
... devenu antidiabétique
Comment le Mediator a-t-il alors pu être commercialisé comme antidiabétique ? Le laboratoire Servier, possédant déjà un coupe-faim sur le marché, utilisera alors, et ce jusqu'au retrait du médicament en 2009, une doctrine selon laquelle le benfluorex possède une « originalité » pharmacologique. Selon lui, le rôle principal du Mediator ne serait pas lié à sa propriété anorexigène, « en réalité très faible et tout à fait accessoire par rapport aux propriétés métaboliques de ce produit », mais serait d'agir sur le métabolisme des lipides et des glucidesglucides. Pour faire oublier son effet coupe-faim, le laboratoire ira même jusqu'à demander, en vain, à changer le nom de la molécule, trop connoté par le suffixe « -orex » qui désigne habituellement les agents anorexigènes.
Le Mediator a été retiré 10 ans trop tard
Plus tard, la fenfluramine sera considérée comme dangereuse et strictement restreinte dans sa prescription en 1995, sans que le Mediator ne soit inquiété. « Si la fenfluramine, toxique, agit principalement par l'intermédiaire de la norfenfluramine, comment ne pas suspecter le benfluorex qui agit, lui aussi, par le biais de la norfenfluramine ? », demandent pertinemment les experts de l'Igas.
Au vu des faits, l'Igas « estime que le retrait du Mediator aurait dû être décidé dès 1999 », soit 10 ans plus tôt que le retrait effectif du médicament. Pourtant, un rapport du laboratoire daté de 1999, faisant volontairement abstraction du rôle prépondérant de la norfenfluramine, n'alertera pas la vigilance de l'Agence française de sécurité sanitaire des produits de santé (Afssaps). Pour conséquence, les patients traités par le Mediator ont donc absorbé de la dangereuse norfenfluramine à des doses efficaces pendant une duréedurée bien trop longue de 33 ans.
Une pharmacovigilance peu vigilante
La seconde responsabilité est donc imputée au réseau de pharmacovigilance, destiné à contrôler l'efficacité et la sécurité des médicaments déjà présents sur le marché. Rappelons qu'aujourd'hui, la situation juridique rend difficile une suspension d'autorisation de mise sur le marchéautorisation de mise sur le marché (AMM) d'un médicament car il faut démontrer, à l'aide de nouvelles données, que le rapport bénéfices/risques est devenu défavorable.
Pour améliorer les choses, il faudrait alors pouvoir analyser et croiser un maximum d'informations médicales concernant les patients sous traitement, notamment en provenance des médecins impliqués dans la pharmacovigilance, des inspections, des contrôles qualité par les laboratoires et de la pharmacoépidémiologie à partir de l'analyse des bases de donnéesbases de données. C'est donc tout le réseau de pharmacovigilance qui est à revoir et qui sera vraisemblablement revu. L'affaire du Mediator aura donc au moins le mérite de faire évoluer un système qui en a besoin.