Les infections à Clostridium difficile répondent mal à l'antibiothérapie. La transplantation fécale semble être une alternative thérapeutique efficace qui réduit significativement les cas de récidives, selon une étude récente réalisée aux États-Unis.
au sommaire
Le microbiote intestinal est une communauté de micro-organismes, essentiellement des bactéries -- et en plus petite proportion, des virus et des champignonschampignons -- qui vit dans notre intestin. Considéré comme un organe à part entière, il intervient dans de nombreux mécanismes physiologiques. Un déséquilibre de cette flore, appelé dysbiose, peut aboutir à l'apparition de maladies ou, tout du moins, favoriser leur émergenceémergence.
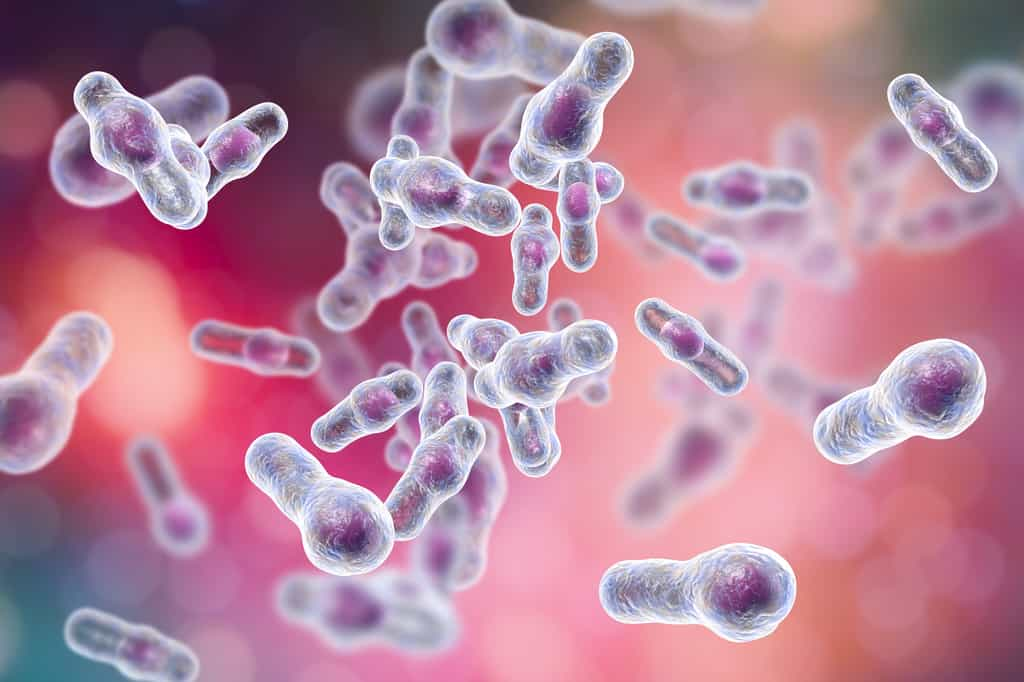
Lorsque que le microbiote intestinal n'est pas aussi divers ni aussi riche qu'il ne devrait l'être, il perd ses capacités protectrices. Des bactéries opportunistes peuvent alors coloniser l'intestin et provoquer des maladies. C'est le cas pour Clostridioides difficile (anciennement Clostridium difficile). Cette bactérie envahit l'intestin à la faveur d'une faiblesse du microbiote intestinal, provoquée par la prise d'un traitement antibiotique, et provoque des troubles intestinaux. C. difficile est un bacillebacille anaérobie stricte, sporulant et producteur de toxinestoxines, les toxines A et B. La première altère la perméabilité de la paroi intestinale et la deuxième détruit les cellules de l'épithéliumépithélium. Leurs actions combinées modifient le transit intestinaltransit intestinal et se traduisent par l'apparition de diarrhéesdiarrhées abondantes à l'odorant caractéristique.
Se débarrasser d'une infection à C. difficile peut devenir un vrai sacerdoce en raison de sa résistancerésistance à l'antibiothérapie, mais aussi par la capacité de la bactérie à entrer en dormance. Les spores permettent aux bactéries de résister longtemps à des conditions défavorables pour leur développement. Lorsque les conditions s'améliorent, des formes végétatives issues des spores réapparaissent. L’infection devient alors chronique. Dans le cas de C. difficile, une infection est considérée comme récidivante lorsqu'elle réapparait huit semaines après le début de l'épisode initiale.
Greffer des selles saines chez les patients malades
Pour venir à bout de ces infections, des chercheurs ont proposé de transplanter le microbiote de patients en bonne santé chez les malades. Connue depuis des millénaires en Chine, la greffegreffe de microbiote a vu ses premiers essais en Occident en 1983, et ces derniers se sont multipliés durant les trente années qui ont suivi pour aboutir, en 2013, au premier essai cliniqueessai clinique randomisé. Ce fut un succès, et aujourd'hui, l'infection à C. difficile est la seule condition pour laquelle la transplantationtransplantation fécale est autorisée.
Dans le journal Gastroenterology, des médecins américains publient les résultats d'une étude observationnelle menée auprès de 259 patients dans 20 hôpitaux différents. Ces patients souffraient d'une infection à C. difficile récidivante et non traitable par l'antibiothérapie. Ils ont subi une transplantation fécale. Pour 9 patients sur 10, l'infection à Clostriodioides difficile a été soignée dans le mois suivant la transplantation fécale avec quelques effets secondaires notables mais peu de récidivesrécidives.
Comme il existe des banques de spermesperme, il existe des banques d'échantillons de selles fournies par des donneurs anonymes. Le patient malade peut ingérer la préparation coliquecolique (c'est-à-dire les selles du donneur) ou elle peut aussi être administrée par coloscopiecoloscopie. C'est cette dernière méthode qu'ont choisie les médecins américains. Sur les 259 patients, 222 ont été transplantés avec environ 250 ml de préparation colique, une seule fois. Les médecins ont ensuite suivi leur état un mois et six mois après l'intervention.
Soigner une infection intestinale en un mois
Seulement un mois après la transplantation, 197 patients sont déclarés guéris de leur infection à C. difficile, soit 98 % de l'effectif initial. Mais de nombreux effets secondaires ont été rapportés, comme des diarrhées indépendantes de l'infection à C. difficile, des douleursdouleurs abdominales, des ballonnements et de la constipationconstipation. La coloscopie est un acte invasifinvasif qui peut servir de porteporte d'entrée à des infections nosocomialesinfections nosocomiales, ce fut le cas pour 2 personnes de l'effectif.
Le suivi à six mois a permis d'observer les cas de récidives : seulement 4 participants, parmi les 122 qui ont été suivis après un et six mois, ont fait une récidive après environ 8 semaines.
Ces observations sont encourageantes puisqu'une seule transplantation fécale a permis de soigner durablement les infections récidivantes à C. difficile et a diminué significativement les récidives qui nécessitent souvent des hospitalisations stressantes pour le patient et coûteuses pour l'hôpital.
La greffe fécale : une nouvelle forme de thérapie ?
Article publié le 29 novembre 2013 par Agnès Roux, Futura
Face aux résistances aux antibiotiques, les médecins sont dans une impasse. Des chercheurs états-uniens confirment l'efficacité de la transplantation fécale pour évincer Clostridium difficile, un germegerme intestinal parfois mortel. Pourrait-on optimiser cette stratégie pour lutter contre certaines maladies chroniques comme le diabètediabète et l'obésitéobésité?
L'histoire semble se répéter. Les chercheurs mettent au point une moléculemolécule miracle contre une infection bactérienne mais le germe trouve rapidement une parade et la rend caduquecaduque. Les staphylocoques, pseudomonas et clostridies sont devenus les bêtes noires des hôpitaux. Malgré les recherches intensives, certains scientifiques sont pessimistes et pensent même que la guerre contre les bactéries est en passe d'être perdue.
En quelques années seulement, la multirésistance aux antibiotiques est devenue un problème de santé publique majeur. Les chercheurs ne perdent cependant pas espoir et font preuve d'une ingéniosité sans faille pour se défendre contre les microbes. Dans une étude récente par exemple, une équipe a fabriqué des nanoéponges capables d'absorber les toxines bactériennes directement dans le sang.

Une autre approche fait progressivement son chemin. Elle n'est pas appétissante mais pourrait fonctionner. Il s'agit de la greffe fécale, autrement dit du dépôt d'une flore intestinaleflore intestinale saine dans un intestin malade pour éradiquer les bactéries pathogènespathogènes. L'idée est simple : lorsqu'une bactérie pathogène pénètre dans le système digestif et se développe, elle perturbe l'équilibre microbien et empêche les gentilles bactéries de venir à la rescousse. En envoyant de nouveaux microbes intestinaux en renfortrenfort, les médecins espèrent exterminer l'envahisseur sans avoir recours aux antibiotiques.
Injecter de nouvelles selles dans un côlon malade
Par cette méthode, on éviterait le problème des résistances aux antibiotiques et on reconstruirait rapidement la flore intestinale indispensable à la santé. Malheureusement, un tel traitement n'est pas sans danger. Il est en effet difficile de déterminer le contenu bactérien exact de la matièrematière fécale récoltée. Il est donc possible que des microbes dangereux y résident et entraînent une nouvelle maladie une fois injectés dans le patient.
Les recherches sur le sujet se focalisent principalement sur l'espèceespèce Clostridium difficile (C. difficile), une bactérie responsable de graves infections intestinales et qui, comme la plupart de ses cousines, a appris à résister à la majorité des antibiotiques utilisés pour la combattre. Dans une nouvelle étude, publiée dans la revue Plos one, une équipe de l'université du Maryland aux États-Unis confirme l'efficacité de la bactériothérapie fécale.
De bonnes bactéries pour vaincre Clostridium difficile
Les chercheurs ont récolté les selles de 14 personnes en bonne santé et les ont analysées afin de vérifier qu'elles étaient dépourvues de parasitesparasites et de bactéries dangereuses comme Salmonella, Shigella, Yersinia ou C. difficile. Ils les ont ensuite déposées dans le côloncôlon de 14 patients infectés par C. difficile avec un cathétercathéter.
Grâce à des technologies de génomiquegénomique et de bioinformatique, les scientifiques ont ensuite analysé la composition microbienne de l'intestin au cours du temps. Ils ont confirmé que la flore intestinale des patients contaminés par C. difficile était beaucoup moins diversifiée que celle des personnes saines, en particulier en ce qui concerne les firmicutes et les protéobacteries. Cependant, une semaine seulement après la transplantation fécale, elle redevient beaucoup plus variée et est même comparable à celle d'une personne non infectée par C. difficile. Mieux encore, les populations bactériennes injectées persistent après une année. Cela signifie que la bactériothérapie dure dans le temps et ne laisse plus l'opportunité à C. difficile de reprendre le dessus.
Une méthode applicable à d’autres maladies ?
Ces travaux confirment l'efficacité de la greffe fécale lors d'une infection par C. difficile. Les perspectives sont multiples. Des études de plus en plus nombreuses révèlent l'importance de la flore intestinale pour la santé. Les milliards de microbes qui nous habitent nous sont en effet bénéfiques à plus d'un titre : ils nous aident à bien digérer, améliorent l'efficacité de notre système immunitaire et influencent le développement de certaines maladies comme l'obésité, le diabète de type 2 et les allergiesallergies. Une étude récente a même montré qu'ils participaient au développement de la dépression !
Ainsi, en contrôlant le microbiote intestinal, les médecins pourraient non seulement vaincre les infections digestives mais également nous protéger contre certaines pathologiespathologies chroniques graves. La transplantation fécale représente une nouvelle forme de thérapiethérapie très prometteuse.