Les médicaments ne sont pas seulement digérés par les enzymes humaines, mais aussi par celles des bactéries de notre microbiote. Une concurrence fâcheuse à l’origine des variations considérables de l’efficacité des médicaments selon les individus, et de certains effets secondaires.
au sommaire
Le métabolisme des médicaments pris par voie orale est fortement influencé par de nombreux facteurs biologiques, en particulier lors de leur passage dans le foie. Mais leur efficacité dépend aussi largement de notre microbiote intestinal. Des chercheurs de l'Université de Harvard viennent ainsi de découvrir que certaines bactéries « mangent » les médicaments avant même qu'ils n'atteignent leur cible.
Un traitement qui demeure mystérieusement inefficace
Les scientifiques se sont intéressés à la Levodopa (L-dopa), un médicament contre la maladie de Parkinsonmaladie de Parkinson introduit dans les années 1960 et chargé d'acheminer la dopaminedopamine vers le cerveaucerveau. Cette moléculemolécule est malheureusement digérée par les enzymesenzymes produites par le corps lors de la digestiondigestion, de telle sorte qu'à peine 1 à 5 % du médicament parvient effectivement au cerveau. Une autre molécule, la carbidopa, a donc été développée pour empêcher la destruction de la L-dopa. Malgré cela, la réponse au traitement demeure hautement aléatoire selon les individus. « Non seulement le traitement n'est pas efficace chez certains patients, mais la L-dopa peut également se tromper de chemin en amenant la dopamine à d'autres endroits que le cerveau, causant ainsi de graves effets secondaires comme des troubles gastriques ou des arythmies cardiaquesarythmies cardiaques », explique Maini Rekdal, l'auteure principale de l'étude parue dans le journal Science le 14 juin.
L’association entre deux bactéries pour saper l’action de la L-dopa
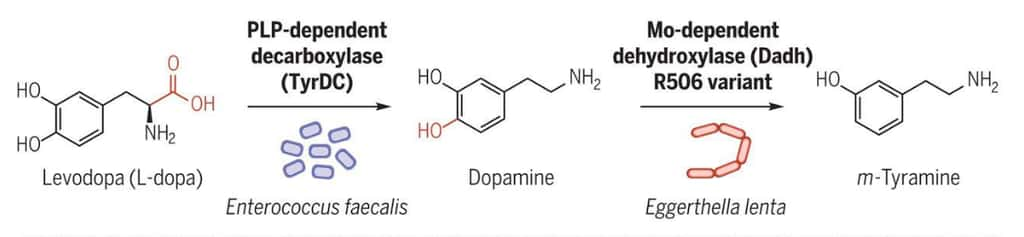
Son équipe vient enfin de comprendre la raison de ce ratage : ce ne sont pas les enzymes digestivesenzymes digestives humaines qui dévorent la L-dopa, mais celles produites par une bactérie du microbiote, Enterococcus faecalis. Celle-ci produit une enzyme qui transforme la L-dopa en dopamine, exactement comme la digestion. Sauf que celles produites par E.faecali semblent légèrement différentes des enzymes humaines, ce qui expliquerait pourquoi la carbidopa n'agit pas contre elles. Les chercheurs ont également découvert une deuxième bactérie, Eggerthella lenta, qui convertit la dopamine en meta-thyramine, un sous-produit potentiellement à la source des effets secondaires observés par la prise de ce médicament. « Tout cela suggère que l'efficacité des médicaments est en grande partie liée au microbiote individuel de chacun », affirme Maini Rekdal.
Les deux tiers des médicaments sont modifiés par les bactéries intestinales
Deux autres récentes études viennent apporter de l'eau à son moulin. La première, parue le 3 juin dans la revue Nature, a analysé l'influence de 76 sortes de bactéries sur 271 molécules actives de médicaments et a découvert que les deux tiers de ces dernières subissaient une modification chimique en présence d'une ou plusieurs de ces bactéries. Ils ont ainsi pu construire une base de donnéesbase de données sur les gènesgènes responsables de ces modifications. La deuxième étude, publiée en février par la même équipe dans Science, montre que certaines bactéries produisent des métabolitesmétabolites hautement toxiques lorsqu'elles sont exposées à des médicaments comme la brivudine (un antiviralantiviral) ou le clonazepam (un antidépresseurantidépresseur).
Ces différentes recherches devraient permettre de personnaliser les traitements selon la flore microbienne de chacun. Des chercheurs envisagent également de modifier le microbiote avec un régime alimentaire spécial afin de doper l'efficacité des médicaments, ou au contraire de limiter les effets secondaires.
Comment la flore intestinale bloque-t-elle l’action des médicaments ?
Article de Agnès Roux publié le 31/07/2013
Certains médicaments sont inactivés par les micro-organismesmicro-organismes contenus dans le tube digestiftube digestif. Des chercheurs viennent d'élucider un mécanisme qui permet à une souche bactérienne de bloquer les effets d'un traitement pour le cœur. Ils ont réussi à enrayer ce processus inhibiteur chez la souris, en modifiant leur régime alimentaire.
Les médicaments pris par voie orale, tout comme la nourriture, glissent jusqu'aux intestins et rencontrent les milliards de microbes intestinaux nichés bien au chaud. Cette flore digestive consomme certains éléments nutritifs que l'organisme ne peut pas digérer, et produit au passage des nutriments essentielsnutriments essentiels à la santé, certaines vitaminesvitamines par exemple.
Mais comment le microbiote intestinal réagit-il à ces médicaments ? De nombreuses études ont montré que les microbes digestifs pouvaient influencer l'action de certains d'entre eux. Les mécanismes se cachant derrière ces processus n'ont pourtant jamais été élucidés. Des scientifiques de l'université Harvard viennent d'apporter quelques éléments de réponse. Dans leur étude, publiée dans la revue Science, ils identifient un mécanisme bactérien permettant de bloquer l'action d'un traitement contre les maladies cardiaques.
Le médicament en question, souvent prescrit en cas d'insuffisance cardiaqueinsuffisance cardiaque, s'appelle le Digoxine. Comme son nom l'indique, il contient la molécule digoxine qui permet d'améliorer le fonctionnement du cœur. « On sait depuis de nombreuses années que cette molécule peut être inactivée par la flore intestinaleflore intestinale », explique Peter Turnbaugh, le directeur de l'étude. En 1980, des chercheurs américains avaient même mis en évidence l'espèceespèce bactérienne responsable de ce phénomène. Il s'agit d'Eggerthella lenta, une bactérie anaérobie installée dans le tube digestif humain.
Deux gènes pour inactiver un médicament pour le cœur
Or, malgré plusieurs années de recherche, les scientifiques n'avaient jamais pu décrypter le mécanisme d'inactivation de la digoxine. Armés des technologies modernes de biologie moléculairebiologie moléculaire, Peter Turnbaugh et son équipe se sont à nouveau attelés à cette tâche. Ils ont cultivé une souche d'E. lenta dans un milieu contenant ou non de la digoxine, et ont analysé les niveaux d'expression des gènes dans ces deux conditions.
Leurs résultats montrent une augmentation importante de l'expression de deux gènes en présence du médicament. « Ce qui est intéressant à propos de ces deux gènes c'est qu'ils codent tous les deux pour des cytochromes, des coenzymescoenzymes qui pourraient très bien inactiver la digoxine. »
Cependant, toutes les souches d'E. lenta ne possèdent pas ces deux gènes à l'origine : la présence de la bactérie chez un individu ne signifie donc pas obligatoirement que le médicament sera inactivé. En revanche, les auteurs ont montré que le niveau d'expression des deux gènes dans des selles était un indicateur de la présence de bactéries inhibitrices de la digoxine. « Nous pouvons ainsi savoir à l'avance si la digoxine sera efficace ou non », annonce le chercheur.
Des protéines pour contrer l’influence de la flore intestinale
Les scientifiques ont approfondi leurs recherches, afin de trouver la faille de la bactérie E. lenta. Des études précédentes avaient montré qu'il était possible de limiter l'action inhibitrice de la bactérie en la cultivant en présence de protéinesprotéines et en particulier de l'acide aminéacide aminé argininearginine. Munis de ces données, ils ont entrepris des expériences chez des souris dotées d'une souche inhibitrice du médicament. Ils les ont traitées avec la digoxine et les ont nourries avec une alimentation riche ou pauvre en protéines. Leurs résultats montrent que l'ingestioningestion de protéines augmente la quantité de médicaments retrouvés dans le sang.
Ces résultats ont permis de décrypter un des processus par lequel les bactéries influencent les thérapiesthérapies cardiaques. En suivant un régime particulier, les patients pourraient alors dompter la flore intestinale et améliorer l'efficacité des traitements médicamenteux. De nombreux travaux restent cependant à faire pour élucider tous les mystères du microbiote intestinal.
Ce qu’il faut
retenir
- La réponse à un même médicament varie fortement selon les individus.
- Les différences s’expliquent notamment par les bactéries du microbiote, qui ingèrent des molécules actives à la place des enzymes humaines ou produisent des sous-produits toxiques responsables d’effets secondaires.