au sommaire

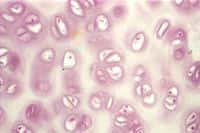
Avec des outils à des prix abordables, on peut synthétiser du tissu humain, comme en atteste cette expérience menée sur le cartilage. Le progrès n'est pas toujours ce qui se fait de plus cher. © Institute of Physics
Un organe défaillant ? La médecine régénérative, celle d'un futur pas si lointain, se donne pour objectif de le dupliquer pour le remplacer. Le principe : recréer artificiellement un tissu organisé à partir de cellules souches en culture. Les avancées dans ce domaine sont fréquentes. Ainsi, des scientifiques ont réussi à façonner des ébauches de foie fonctionnel ou d'œil à partir de simples cellules souches.
À chacun sa méthode. Et certains se laissent tenter par un outil banal : l'imprimante. Combinée à une machine à électrofilageélectrofilage, des scientifiques américains du Wake Forest Institute for Regenerative Medicine (WFIRM) ont synthétisé un cartilage artificiel capable d'assurer pleinement sa fonction lorsqu'on l'implante chez l'animal. L'utilisera-t-on un jour chez l'Homme ?
Une imprimante à jet de chondrocytes
L'idée n'est pas nouvelle puisque des chercheurs se sont déjà risqués à fabriquer du cartilage à partir d'une imprimante à jet d’encre... ou plutôt à jet de chondrocytes. En effet, des couches successives de ces cellules du cartilage associées à de l'hydrogelhydrogel et à du collagène étaient assemblées de manière à donner une structure tridimensionnelle. Cependant, celle-ci manquait de rigiditérigidité et de stabilité. Il fallait donc améliorer le processus.
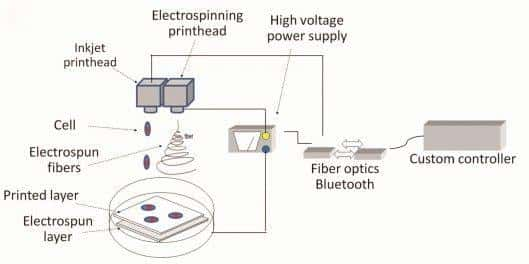
Ce schéma reprend le principe de fonctionnement de l'imprimante 3D de cartilage. Derrière sa console (Custom controller), l'utilisateur personnalise sa production. Le signal est envoyé via Bluetooth ou fibre optique à deux têtes d'impression. D'abord, un générateur électrique (High voltage power supply) stimule la tête d'impression à électrofilage (Electrospinning printhead) pour qu'elle synthétise un squelette en fibres de polymères (Electrospun fibers). Cette structure passe sous la tête d'impression à encre (Inkjet printhead). Elle contient des cellules de cartilage (Cell) qui vont occuper les trous. Couche après couche, la structure prend forme. © Institute of Physics
Comme expliqué dans la revue Biofabrication, l'imprimante est couplée à une machine à électrofilage. Elle permet de générer des fibres extrêmement fines à partir d'une solution de polymèrespolymères liquidesliquides. Ces lamelles de 400 µm d'épaisseur sont assemblées pour constituer l'équivalent du squelette de la structure, qui est poreuse. On passe les couches les unes après les autres dans une imprimante qui va remplir les trous avec un gelgel de chondrocytes récupérés dans les oreilles de lapin, avant d'empiler le tout pour obtenir la forme désirée.
Du cartilage artificiel dans les articulations humaines
Une semaine après, les cellules de cartilage étaient toujours vivantes, alimentées par des moléculesmolécules contenues dans le gel. Plus intéressant : ce cartilage artificiel semble biocompatible. Injecté chez des souris, la transplantation a pris et au bout de huit semaines, il présente les mêmes propriétés et structures qu'un cartilage élastique naturel.
La suite logique de cette expérience est de tester cette structure chez l'Homme. Chez des patients avec des troubles articulaires comme l'arthrose, l'idée est de prendre par IRMIRM une image de l'articulationarticulation douloureuse. Ainsi, on pourrait modéliser la forme de la structure cartilagineuse à créer avant de la passer à la machine et de l'implanterimplanter.
Certains imaginent déjà le remplacement des chondrocytes par des cellules souches pluripotentes induitescellules souches pluripotentes induites (CSPi). Pour cela, il est nécessaire de prélever des cellules de la peau du patient. On inverse l'évolution des cellules et on les pousse à retourner dans un état indifférencié. Ensuite, on contrôle leur différenciation pour les transformer en chondrocytes. Ces cellules étant dotées du patrimoine génétiquegénétique du patient, on serait certain d'éviter tout problème de rejet.