au sommaire
La médecine personnalisée se fait peu à peu une place dans le secteur des biotechnologiesbiotechnologies. Elle permet un meilleur ciblage de la maladie et un accompagnement plus efficace du patient grâce au recueil et à l'analyse des données. Bientôt, elle pourrait notamment jouer un rôle majeur dans la lutte contre le cancercancer.
Le docteur Jean-Pierre Armand est consultant en oncologieoncologie à l'Institut Gustave Roussy. Ancien directeur général de l'Institut Claudius Regaud, il a présidé l'European Society for Medical Oncology. Jacques Biot est président exécutif de l'École polytechnique. Il a occupé des fonctions exécutives au sein d'entreprises françaises de biopharmacie avant de devenir entrepreneur et investisseur dans le domaine des sciences de la vie.
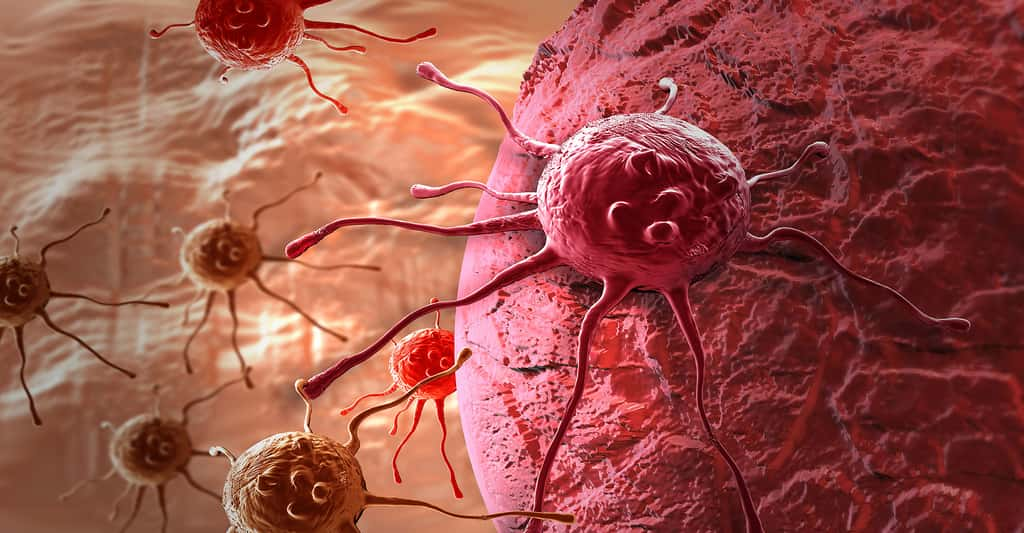
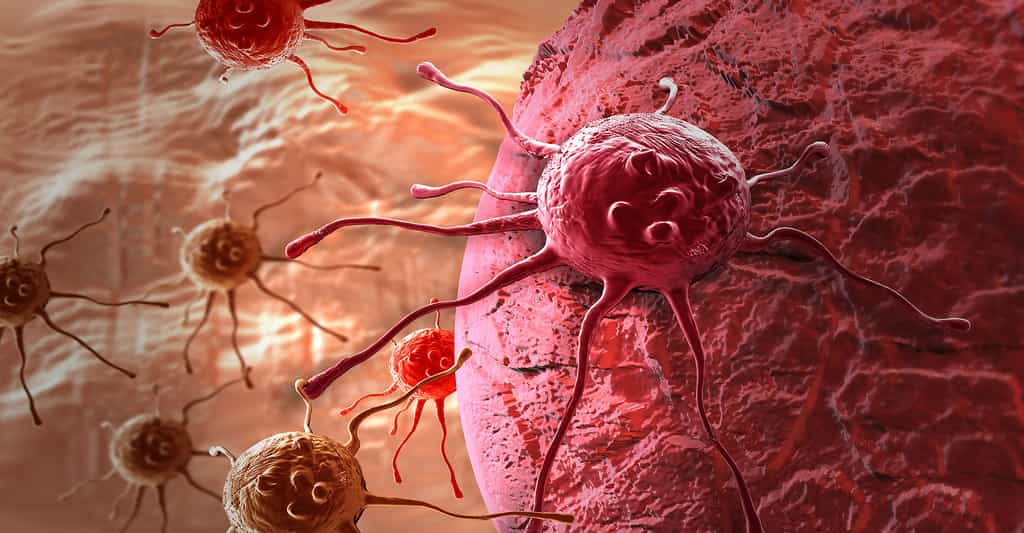
Le développement des biotechnologies médicales et de la médecine personnalisée pourrait notamment jouer un rôle essentiel dans le traitement des cancers. Ici, des cellules cancéreuses. © Jovan Vitanovski, Shutterstock
Chaque maladie et chaque cas sont-ils uniques ?
Jacques Biot : Chaque maladie n'est pas unique, mais chaque malade est unique.
Jean-Pierre Armand : Oui. À l'extrême, chaque maladie pourrait être unique, en particulier si l'on intègre l'environnement des défenses de l'individu, mais nous ne sommes pas encore à ce niveau-là. Aujourd'hui, on stratifie le cancer du seincancer du sein en 15 cas différents. Demain, ça sera 30 et après-demain, cela pourrait être une situation où l'on interviendrait pour chaque malade porteur d'une maladie raremaladie rare.
Sur quels outils la médecine personnalisée s’appuie-t-elle ?
J. B. : Si son concept est simple, sa mise en œuvre est complexe. L'outil fondamental est le diagnosticdiagnostic. Non moins fondamental est le protocoleprotocole qui lie, à un diagnostic donné, la prise en charge adaptée. L'un comme l'autre nécessitera pour sa démonstration des évolutions méthodologiques qui conditionneront la large diffusion du concept.
J.-P. A. : Les cancers cliniques sont décrits très tôt dans l'histoire de l'humanité, mais c'est l'apparition du microscopemicroscope, lunette astronomique inversée, qui a été l'outil diagnostique clé. Les outils d'analyse sont indispensables pour progresser, recueillir l'information et avoir une parfaite connaissance de la tumeurtumeur, très hétérogène. L'analyse moléculaire de la tumeur n'a été possible que par l'invention des outils de séquençageséquençage, permettant une nouvelle classification plus précise des cancers.
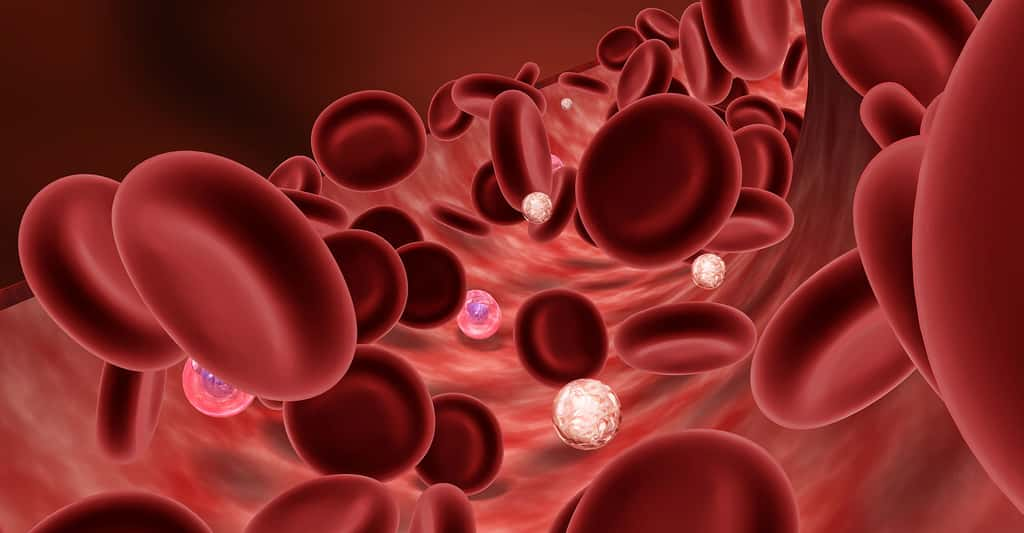
Les lymphocytes sont des leucocytes (globules blancs) qui ont un rôle majeur dans le système immunitaire. Sur l'image, les leucocytes sont les petites sphères blanches parmi les globules rouges. © BioMedical, Shutterstock
Cependant, dans la tumeur, il y a des cellules cancéreuses propres avec des mutations et des anomaliesanomalies que l'on commence à bien connaître et, tout à côté, un immense domaine - que l'on a sous-évalué à ce jour - qui est tout l'environnement non cancéreux (telles les cellules immunologiquement compétentes, bloquées, qui ne peuvent pas faire leur travail).
L'intégration de tous ces paramètres - les infiltrations de lymphocyteslymphocytes, l'environnement vasculaire de la tumeur - constitue des données, de qualité très moyenne, pour lesquelles nos outils d'analyse sont très médiocres. Le recueil précis de l'ensemble de ces données va jouer un rôle majeur dans les conclusions que l'on prendra. Si les données sont médiocres, la conclusion sera incertaine et reposera encore sur des conclusions probabilistes. En effet, dans un deuxième temps, l'outil biomathématique permettra d'analyser ces grandes quantités de données pour leur associer un nombre limité de molécules.
Pourquoi ces données sont-elles de qualité « encore très moyenne » ?
J.-P. A. : Tout le monde croit qu'il suffit de prendre un petit morceau de tumeur, de le mettre dans un tube et de le faire passer dans un instrument d'analyse pour que tous les secrets en soient révélés avec précision, comme pour une simple glycémieglycémie. La reproductibilité de toutes ces analyses est, hélas, loin d'être aussi précise. La qualité de nos données est encore très moyenne car les tumeurs sont hétérogènes : leur profil varie avec le temps et l'environnement permet leur développement. Quatre métastasesmétastases issues d'organes différents auront des profils sensiblement distincts et souvent différents de celui provenant de la tumeur primitive analysée quatre ans auparavant.
Quels progrès permet la médecine personnalisée ?
J. B. : Il y a trois axes majeurs de progrès : l'efficacité, la tolérance et l'économie. Ils se nourrissent les uns des autres. La médecine statisticienne du siècle dernier, qui administrait à de nombreux patients « non répondeurs » des traitements inutiles et mal tolérés, a un coût supporté par la collectivité.
J.-P. A. : On peut citer l'exemple du projet ALK, du nom d'un gènegène initialement mis en place pour le traitement d'un cancer du sangcancer du sang : on s'est aperçu que ce gène était présent dans 4 % des cas de cancer du poumoncancer du poumon. Grâce au médicament mis au point, on peut traiter ces cas de façon ciblée. Le crizotinib assure 95 % de réponse chez les malades porteurs de la mutation ALK. Seuls 5 % des malades seront exposés à une toxicitétoxicité incontournable. L'efficacité a été optimale, la toxicité clinique et « financière » a été évitée aux malades non répondeurs au traitement. Parmi les cancers du poumon, on peut donc la qualifier de maladie rare. Pourtant, avec un petit nombre d'essais thérapeutiquesessais thérapeutiques, elle a bénéficié d'un développement très rapide grâce à une médecine de précision qui a identifié un biomarqueur spécifique.
Avec cette approche de la médecine, quelle est la place de la France à l’international ?
J. B. : Sur le versant médical, la tradition pasteurienne de la France maintient une légitimité solide. Sanofi, le principal industriel national, a certes longtemps tourné le dosdos aux biotechnologies, mais il a regagné sa place de leader en ce domaine. Je me réjouis qu'il coproduise le premier anticorpsanticorps monoclonalmonoclonal au monde indiqué dans le traitement de l'hypercholestérolémiehypercholestérolémie, le Praluent (alirocumab). Sur le versant chirurgical, la France n'a pas su constituer un acteur industriel global. Toutefois, il y a un foisonnement de créations d'entreprises de technologies médicales de pointe, à l'initiative conjointe de nos chirurgiens et de nos ingénieurs. Ces projets sont ralentis dans leur développement par la faible ouverture du marché français à l'innovation, notamment pour des raisons tarifaires (difficulté d'accéder au remboursement).
Dans le diagnostic, l'Institut Mérieux joue un rôle de premier plan. Cependant, le secteur du typage génétiquegénétique, à la croissance la plus prometteuse, reste dispersé et largement contrôlé par les laboratoires intégrés dans les hôpitaux, alors que d'autres pays ont autorisé la création de leaders industriels.
J.-P. A. : Il faut certes différencier la recherche et l'industrie pharmaceutique françaises. Si la fin du XXe siècle a reconnu une place privilégiée à la France dans la recherche de traitements des cancers, il faut reconnaître que le pays a manqué l'accélération observée ces quinze dernières années avec la médecine de précision. Les perspectives semblent s'améliorer grâce à l'extraordinaire dynamisme des biotechs françaises. Il aura fallu un demi-siècle après la découverte des microbesmicrobes pour qu'Alexander FlemingAlexander Fleming nous offre la pénicillinepénicilline. Il faut aujourd'hui quatre années entre la découverte d'une nouvelle cible thérapeutique et la mise à disposition d'un traitement. Le saut conceptuel de l'immunothérapieimmunothérapie constitue un virage radical.
Nous avons eu deux prix Nobel en immunologie et si nous défendons une recherche de rupture dans ce domaine nous retrouverons notre place. Dans la tumeur, par exemple, les cellules immunologiquement compétentes reconnaissent une cellule cancéreuse comme étrangère. Leur manipulation donne des résultats encore limités, mais qui bouleversent nos concepts thérapeutiques : 20 % des malades à un stade très avancé sont sensibles au traitement et 5 % semblent guéris sans traitement à cinq ans. Les outils diagnostiques et thérapeutiques de cette approche sont encore à découvrir dans ce domaine.