au sommaire

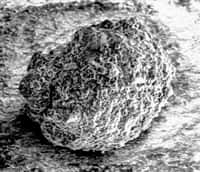
Le chrome se présente sous la forme d'un métal gris acier et dur. © Alchemist-hp, Wikimedia Commons, CC by-nc-nd 3.0
Le chrome, le métal de transition qui fait rutiler les pare-chocs, est aussi très présent dans les peintures. Son nom fait d'ailleurs référence à la couleur.
Généralités
- Symbole : Cr
- Numéro atomique : 24
- Électrons par niveau d'énergie : 2, 8, 13, 1
- MasseMasse atomique : 51,9961 u
- IsotopesIsotopes les plus stables : 52Cr stable avec 28 neutronsneutrons (83,789 %), 53Cr stable avec 29 neutrons (9,501 %), 54Cr stable avec 30 neutrons (2,365 %), 50Cr avec une demi-viedemi-vie supérieure à 180 millions de milliards d'années (4,31 %)
- Série : métauxmétaux de transition
- Groupe, période, bloc : 6, 4, d
- Densité : 7,15
- Point de fusionfusion : 1.907 °C
- Point d'ébullition : 2.671 °C
Historique du chrome
L'emploi du chrome dans certains objets métalliques est attesté en Chine voilà deux millénaires. C'est en 1798 que fut isolé le chrome métallique, par Nicolas Louis Vauquelin. Le nom « chrome » vient du grec chroma signifiant « couleur » car les composés du chrome sont extrêmement colorés.
Propriétés du chrome
Le chrome se présente sous la forme d'un métal gris acieracier et dur. Sa principale particularité est de résister au ternissement et à la corrosioncorrosion. Les états d'oxydationoxydation de +2 à +6 sont rencontrés. Le chrome hexavalent est particulièrement oxydant tandis que le chrome (II) est un réducteur.
Utilisation du chrome
L'utilisation du chrome la plus connue est sans doute en métallurgie, pour donner un rendu brillant en plus d'améliorer la résistancerésistance à la corrosion. On emploie aussi le chrome comme catalyseurcatalyseur dans certaines hydrogénationshydrogénations. Les chromates, par leurs couleurs variés (nuances de jaune pour le chromate de plombplomb) se retrouvent dans les peintures, mais ils sont toxiques. Dans les verresverres, les sels de chrome ajoutent une touche de vert.

Les effets du chrome sur la santé
Le chrome est un métal toxique pour l'Homme, notamment le chrome (IV). Sa toxicitétoxicité est fortement dépendante de sa forme : nanoparticulenanoparticule, oxyde, valencevalence, etc. Il est bioaccumulé dans certains organismes, comme des végétaux alimentaires. De ce fait, il peut altérer la santé humaine. Néanmoins, le chrome (III) est essentiel pour l'Homme comme nutrimentnutriment, dont la carencecarence peut avoir des conséquences cardiaques ou encore sur le diabètediabète. L'excès de chrome (VI) inhalé provoque des saignements de neznez ou encore des irritations nasales.
Son mode d'action n'est pas encore totalement élucidé, mais on sait que le chrome agit comme cofacteur de l'insulineinsuline, facilitant ainsi l'assimilation du glucoseglucose par les cellules.
- Valeur de référence dans la population générale : Cr sérique < 0,5 µg/L.
- L'absorptionabsorption dépend de sa solubilité et de sa valence : les dérivés trivalents sont, en général, plus faiblement absorbés que les dérivés hexavalents. Le chromate de potassiumpotassium, de sodiumsodium et de lithiumlithium sont tous trois solubles. Les chromates non alcalins, insolubles, sont le chromate de plomb, de strontiumstrontium et de zinczinc.
- Les dérivés solubles du chrome VI pénètrent dans l'organisme par toutes les voies, respiratoires en milieu professionnel, digestives (défaut d'hygiène) et percutanées.
- Le chrome se distribue dans le foiefoie, les reinsreins, la raterate et le poumonpoumon.
- L'excrétion est essentiellement urinaire sous forme de chrome III (> 80 %) et faiblement fécale.
- InterférencesInterférences, interprétation : le tabac, la consommation de bière, l'hygiène personnelle, l'état cutanécutané, les modes de travail et surtout la valence, la solubilité et la forme physiquephysique du chrome sont à prendre en compte.

Quelques aliments riches en chrome : le foie de veau, les céréalescéréales complètes, le fromage, les prunesprunes, les brocolisbrocolis, les haricots vertsharicots verts, la bière. Il semble que l'agricultureagriculture intensive et le raffinageraffinage réduisent la teneur en chrome des aliments.
Le chrome et l'industrie
Le chromage dur : le plus glissant, et un des plus durs, des revêtements anti-usure. D'un excellent rapport qualité-prix, il permet la protection de pièces neuves et le rechargement de réparation.
Le chrome dur est un revêtement par électrolyseélectrolyse qui s'applique sur tous types de supports : acier, inoxinox fontefonte, alliagesalliages cuivreux, bronzebronze, aluminiumaluminium etc.
On retrouve le chrome dur dans tous les secteurs d'activités : automobileautomobile, sidérurgie, mécanique, agroalimentaire, aéronautique, hydraulique, imprimerie, verrerie, fonderie, travaux publics, métallurgie, recyclagerecyclage déchetsdéchets industriels, papeterie, pneumatiquepneumatique, textile, plasturgieplasturgie, outillage, médical, etc.
Il résiste à pratiquement tous les agents chimiques (sauf acide chlorhydriqueacide chlorhydrique), même à haute température. Il est inoxydable jusqu'à 800 °C. Sa duretédureté exceptionnelle est de 1.000 à 1.100 vickers.
Le coefficient de frottement chrome/acier est diminué de moitié par rapport au coefficient acier/acier. Le chromage dur offre un très bel aspect et adhère très bien à son support (accroche moléculaire). Les lignes de chromage dur récentes totalement informatisées peuvent atteindre des capacités de bains de 50.000 litres.

Le chrome et la pollution
Un exemple à Genève avec cet extrait du site officiel de la ville de Genève :
« Le 19 décembre 2000, monsieur Cramer, conseiller d'État, chargé du département de l'intérieur, de l'agriculture, de l'environnement et de l'énergie, a rappelé l'importance de l'établissement d'un cadastrecadastre des sites contaminés à l'occasion de la présentation d'un cas de site nécessitant un assainissementassainissement rapide.
Des fouilles et des forages ont été réalisés sur la parcelle et des échantillons de sol ont été analysés. Les résultats de ces analyses montrent que la pollution du sol par le chrome VI est localisée principalement sur la parcelle. La concentration est très importante sous le dallage de l'atelier de chromage (326 mg/kgkg) et elle diminue en profondeur (5,4 mg/kg à 6 mètres de profondeur). Des pollutions d'extension et d'intensité plus limitées ont également été mises en évidence par les analyses, notamment pour les cyanures et d'autres métaux lourds (plomb, cadmiumcadmium, zinc). Un forage a été réalisé, en limite de la parcelle, pour prélever l'eau de la nappe souterraine et effectuer des analyses. Les concentrations de Cr VI mesurées (max. 0,29 mg/l, min 0,14 mg/l) démontrent clairement que la nappe d'eau souterraine est atteinte localement, que le site est contaminé et qu'il y a nécessité d'assainir. »

Un autre exemple dans l'Oise ainsi qu'à la Réunion :
« Cas de la nappe de la craiecraie de la vallée de l'ArondeAronde (Oise) : une langue de pollution ponctuelle par le chrome hexavalent (de 2 km de long sur 200 m de large) a contaminé un captage public, suite aux rejets des eaux de rinçage et de bains par une usine de chromage dans un bassin et un puisardpuisard. Les concentrations en ce métal lourd variaient de 3,5 mg/L en amont à 0,8 mg/L en aval. Après cinq ans de pompage de dépollutiondépollution, les valeurs au captage ont chuté de 0,4 mg/L à 0,005 mg/L. » (Mme A. Desbordes - Pollutions des eaux souterraines en Picardie. Mém. Maîtrise BG, Fac. Sciences, Amiens, 50 p. + annexes.-2000-).

Les sols de la Réunion, entre autres, sont très riches en éléments traces métalliques, des micropolluants potentiels des rivières, des sols et de nos assiettes. Une équipe du Cirad a récemment démontré que ces éléments ont, sur l'île, une origine naturelle. Aujourd'hui, des travaux portent sur l'étude de leur mobilité ainsi que sur les risques de toxicité dans l'alimentation. (Cirad, La recherche agronomique au service des pays du sud, voir bibliographie)
La toxicité du chrome
L'Organisation mondiale de la santéOrganisation mondiale de la santé a fixé à 0,050 mg par litre la concentration de Cr6 à ne pas dépasser dans les eaux.
La plupart du chrome de l'airair se dépose et finit dans l'eau ou dans le sol. Dans le sol, le chrome se lie aux particules du sol et ne se déplace pas jusqu'à l'eau souterraine. Dans l'eau, le chrome est adsorbé sur les sédimentssédiments et s'immobilise, seule une très petite partie se dissout. L'eau transporte les métaux lourds, et les incorpore dans la chaîne alimentairechaîne alimentaire (alguesalgues → planctonplancton → poissonpoisson, etc.). Même si les métaux lourds sont présents à l'état de traces, ils sont très dangereux à cause de la bioaccumulationbioaccumulation dans les organismes.
Une intoxication aiguë peut provoquer une tubulonéphrite : blocage rénal. Une intoxication chronique entraîne des lésions cutanées et muqueusesmuqueuses avec atteinte respiratoire allant jusqu'au cancercancer bronchopulmonaire.
« Dans les eaux littorales, la contaminationcontamination par le chrome est plus importante dans la phase particulaire que dans la phase dissoute. Les fleuves les moins contaminés présentent des concentrations en chrome dissous de l'ordre de 1 à 2 µg/l. En ce qui concerne le milieu aquatique, les organismes inférieurs sont plus sensibles que les poissons. De plus, le chrome hexavalent, qui est toxique pour la faunefaune aquatique d'eau douceeau douce à une concentration relativement élevée, est peu toxique dans l'eau salée. » (Ifremer Monographie littorale de Basse-Normandie).
Sources :
- C. König : cours personnels (chimiechimie et environnement) ;
- L'eau aujourd'hui, Editions Georg, Genève ;
- Documents Ifremer ;
- Documents OMS ;
- Lenntech : purification et traitement de l'eau ;
- Cirad.