Être capable de produire de l’oxygène à partir de ressources naturellement présentes sur la Lune semble indispensable à la future colonisation de notre satellite. Et des ingénieurs de l’Agence spatiale européenne (ESA) annoncent aujourd’hui être sur la bonne voie. Grâce à leur centrale test, ils sont capables d’extraire l’oxygène contenu dans le régolithe lunaire.
au sommaire
Sur la Lune, les impacts de météorites ont laissé derrière eux une couche de poussières que les astronomesastronomes appellent le régolithe. Il a tendance à provoquer toutes sortes de problèmes techniques aux engins qui se posent sur notre satellite. Il pourrait aussi causer des problèmes de santé aux astronautes qui doivent retourner prochainement sur la Lune. Mais les ingénieurs l'envisagent aujourd'hui surtout comme une ressource naturelle abondante.
Il y a quelques mois, ils imaginaient construire avec, les briques des futures bases lunaires. Et pourquoi ne pas en extraire l’oxygène nécessaire aux prochains explorateurs de notre satellite ? L'Agence spatiale européenne (ESA) annonce même avoir installé, au cœur de son Centre européen de technologie spatiale (Pays-Bas), une centrale prototype destinée à montrer la faisabilité de ce dernier projet.
Les échantillons de régolithe que de précédentes missions ont ramenés de la Lune confirment que le matériaumatériau est composé de 40 à 45 % d'oxygèneoxygène en poids. L'ennui, c'est que, dans le régolithe, l'oxygène apparaît sous forme d'oxydes, chimiquement lié à d'autres éléments. Et donc, non disponible.

Une centrale à oxygène pilote, dès le milieu des années 2020
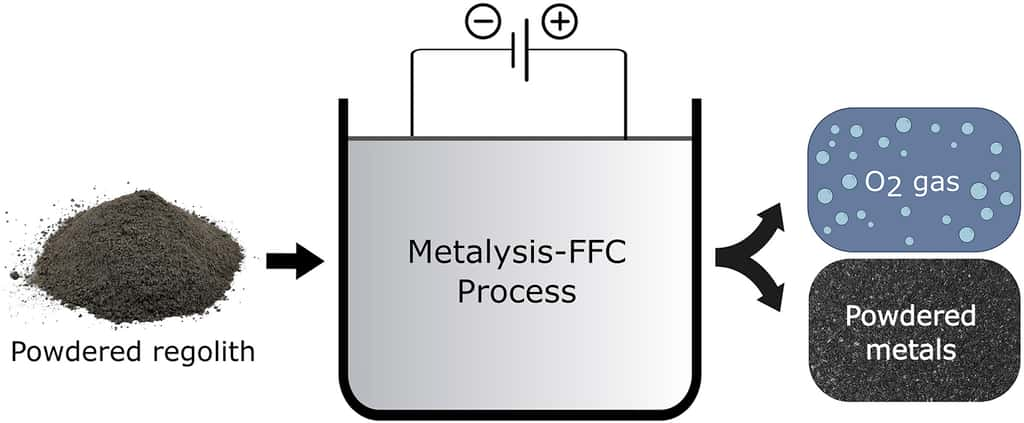
Ainsi, pour extraire l'oxygène du régolithe lunaire, les ingénieurs de l'ESA comptent sur une technique appelée l'électrolyseélectrolyse en milieux de sels fondus. Le régolithe est placé dans une enceinte en métal contenant du chlorure de calcium (CaCl2) fondu. Le tout est chauffé à 950 °C. Le régolithe demeure solidesolide. Mais lorsque l'on y fait passer un courant, l'oxygène est extrait et migre à travers le sel pour être collecté du côté de l'anodeanode. En parallèle, le restant de régolithe est également converti en alliagesalliages métalliques.
D'autres techniques existent. Mais elles se révèlent moins rentables ou demandent de monter à des températures de plus de 1.600 °C. Cette technique semble la plus prometteuse. Elle est d'ailleurs déjà exploitée industriellement. Mais pas pour la production d'oxygène qui, dans ce cas, fait plutôt figure de sous-produit indésirable. Il a donc fallu, aux ingénieurs de l'ESA, imaginer un tuyau d'échappement pour permettre de libérer l'oxygène en un point donné. Dans les prochaines évolutions, il est prévu, bien sûr, que l'oxygène soit stocké en sortie de process.
“Extraire 96 % de l’oxygène du régolithe”
Comme l'objectif est de renvoyer des Hommes sur la Lune dans les années à venir, pour y demeurer, cette fois, l'idée est bien de peaufiner la technologie. Pour en réduire la température de fonctionnement, par exemple. Et pour faire la démonstration d'une usine pilote d'ici le milieu des années 2020. Pour l'heure, les ingénieurs de l'ESA affirment être capables d'extraire 96 % de l'oxygène du régolithe en 50 heures d'opération. Mais déjà 75 % en seulement 15 heures.
Colonisation de la Lune : une méthode prometteuse pour y produire de l'oxygène
Le régolithe lunaire contient des oxydes métalliques en abondance et l'on sait depuis des décennies que l'on pourrait extraire d'importantes quantités d'oxygène de ce sol. Une méthode particulièrement prometteuse par électrochimie a finalement été mise au point, fournissant en bonus des alliages métalliques. Elle sera peut-être utilisée par les futurs colons lunaires.
Article de Laurent SaccoLaurent Sacco paru le 14/10/2019

Une base lunaire aurait bien des avantages. Le champ de gravitégravité de la Lune étant plus faible que celui de la Terre, l'extraction de matériaux permettant de construire les fameuses colonies spatiales de Gerard O'Neill y serait plus aisée. Avec une biosphèrebiosphère en réduction, elle permettrait de tester certains des concepts nécessaires à l'établissement d'une base permanente et autonome pour des colons martiens. Mais pour cela, il faudrait pouvoir faire vivre une population humaine non négligeable et cela implique de pouvoir disposer de ressources en oxygène et en eau.
Nous avons de bonnes raisons de penser qu'il existe des ressources en eau dans certains cratères lunaires aux pôles. Mais nous ne savons pas en pratique si elles seront vraiment adaptées à la colonisation.
En ce qui concerne l'oxygène, nous savons depuis les travaux de pionniers, dans les années 1960, qu'il est possible de l'extraire du sol lunaire. En effet, le régolithe et les roches sur la Lune contiennent beaucoup d'oxygène sous forme d’oxyde métallique de fer, de titane et bien sûr de silicium, formant des minéraux. Au cours des décennies qui ont suivi le programme Apollo, une vingtaine de processus physico-chimiques ont été proposés pour produire de l'oxygène sur la Lune.
Une présentation des études faites par l'ESA sur le régolithe lunaire. Pour obtenir une traduction en français assez fidèle, cliquez sur le rectangle blanc en bas à droite. Les sous-titres en anglais devraient alors apparaître. Cliquez ensuite sur l'écrou à droite du rectangle, puis sur « Sous-titres » et enfin sur « Traduire automatiquement ». Choisissez « Français ». © European Space Agency, ESA
Des procédés pour extraire l'oxygène du sol lunaire avec l'énergie solaire
Parmi les plus étudiés, avec diverses variantes, on trouve ceux consistant à utiliser une sorte de four solaire avec des miroirsmiroirs concentrant les rayons du SoleilSoleil pour porter à des températures élevées (entre 700 et 1 000 °C) du régolithe ou des roches, éventuellement collectés et amenés dans le four par des robotsrobots. Certains minérauxminéraux - comme l'ilménite de formule FeTiO3 - peuvent alors réagir avec de l'hydrogènehydrogène ou du méthane pour produire presque directement de l'oxygène ou du monoxyde de carbonemonoxyde de carbone et de l'hydrogène. À plus basse température, le monoxyde de carbone et l'hydrogène donnent alors du méthane et de l'eau que l'on peut électrolyser pour obtenir de l'oxygène et de l'hydrogène. Méthane ou hydrogène, selon la réaction de départ, peuvent donc être réutilisés pour boucler un cycle de production d'oxygène. Il faudrait bien sûr apporter suffisamment de méthane ou d'hydrogène en provenance de la Terre pour amorcer un tel cycle.
Une autre grande classe de processus repose, elle, sur l'électrolyse d'un bain de roches lunaires silicatées fondues. Dans les deux cas de figure, on a besoin d'énergieénergie solaire pour chauffer et produire de l'électricité, ce qui ne devrait pas poser de problème sur la Lune. L'électricité pourrait, de plus, servir à alimenter des sortes de catapultes magnétiques qui permettraient d'envoyer dans l'espace, aussi bien des réserves d'oxygène liquideliquide, pour des colonies spatiales ou pour la propulsion de vaisseaux en orbiteorbite destinés à exploiter les astéroïdes, que des matériaux issus de l'industrie lunaire, par exemple les métauxmétaux produits indirectement par l'extraction de l'oxygène.
L'ESA vient de faire savoir qu'une nouvelle technique d'électrolyse très prometteuse venait d'être découverte par une chimiste de l'université de Glasgow, Beth Lomax, dont les recherches doctorales ont été soutenues par l'agence européenne. Beth Lomax et ses collègues ont d'ailleurs publié leurs travaux à ce sujet dans un article du journal Planetary and Space Science.
L'idée derrière la nouvelle méthode électrochimique est une variante de celle développée depuis sa découverte en 1996-1997 à l'université de Cambridge par George Chen, Derek Fray and Tom Farthing. Elle est pour cette raison connue sous le nom de procédé FFC et ses découvreurs ont vendu le brevet à des entrepreneurs canadiens et britanniques, James Reimer et Ray Power, qui ont fondé une entreprise pour exploiter son potentiel : Metalysis. Le procédé FFC permet d'exploiter des composés métalliques solides, en particulier des oxydes, qui sont réduits de manière cathodique en métaux ou alliages respectifs à partir de sels fondus.
Beth Lomax a conduit ses recherches aussi en association avec Metalysis. Les échantillons de roches lunaires étant trop précieux pour ce genre d'expérience d'extraction de l'oxygène à partir des oxydes métalliques du régolithe lunaire (rappelons que celui-ci contient de 40 à 45 % de son poids en oxygène), c'est du sol lunaire artificiel qui a été utilisé. Nous pouvons avoir confiance dans la fidélité de ce sol simulé puisque justement les centaines de kilogrammeskilogrammes d'échantillons lunaires rapportés par le programme Apollo nous ont permis de bien connaître le régolithe lunaire.

De l'oxygène mais aussi des métaux pour les colons lunaires
Dans le procédé mis au point par Beth Lomax, un courant électriquecourant électrique parcourt un mélange d'une poudre de régolithe simulé dans du chlorure de calciumcalcium fondu à 950 °C de sorte que le régolithe demeure solide. La chimiste précise d'ailleurs à ce sujet que : « C'est le premier exemple de traitement direct "poudre à poudre" du régolithe lunaire solide simulé capable d'en extraire la quasi-totalité de l'oxygène. Les méthodes alternatives d'extraction de l'oxygène lunaire permettent d'obtenir des rendements nettement inférieurs ou nécessitent la fusionfusion du régolithe à des températures extrêmes, supérieures à 1 600 °C. »
Le nouveau procédé semble vraiment efficace et prometteur. Pour s'en convaincre, on peut déjà dire qu'il suffit de 50 heures pour extraire 96 % de l'oxygène contenu dans un échantillon de régolithe, mais seulement 15 heures pour en extraire déjà 75 %.
En ce qui concerne les applicationsapplications pour la métallurgie, on obtient trois groupes d'alliages principaux (parfois mélangés à de petites quantités d'autres métaux) à savoir deux alliages |e5313f56b7041a07b29d6983a4edb33e|-aluminiumaluminium et le fer-siliciumsilicium et un autre de type calcium-silicium-aluminium. Surtout, ces alliages se présentent comme des phases facilement séparables, ce qui est favorable à des processus de raffinement permettant d'obtenir du fer, de l'aluminium et du calcium à l'état pur in fine.
En bonus, il n'y a pas de raison pour que la méthode utilisée ne soit pas transposable au régolithe martien.

Produire de l'oxygène sur la Lune
Article de Rémy DecourtRémy Decourt publié le 19/06/2005
Dans le cadre de la Nouvelle Vision de l'Espace, un ambitieux projet initié par le président Bush d'exploration spatiale, qui prévoit de retourner sur la Lune avant d'aller sur Mars, la NASANASA vient d'octroyer un contrat portant sur le développement de technologies capables de produire de l'oxygène à partir du régolite lunaire, cette couche poussiéreuse qui recouvre la surface de notre satellite naturel.
Les bénéficiaires de ce contrat sont Florida Tech, British Titanium, l'université de Cambridge et le Centre spatial Kennedy de la NASA.
L'oxygène est l'élément le plus abondant des roches lunaires mais un processus d'extraction est nécessaire avant d'envisager son utilisation. La NASA est engagée dans plusieurs projets qui visent tous à mettre au point un appareil capable de transformer la poussière lunaire en oxygène. L'Université de Cambridge et son laboratoire de Science des matériaux et métallurgie sont en pointe dans ce domaine d'où l'intérêt que leur porteporte la NASA.
Ce contrat vise à produire de l'oxygène à partir d'un processus mis au point par l'Université de Cambridge et connu sous le nom de Fray-Farthing-Chen (FFC) Cambridge qui utilise la réduction électrochimique d'oxydes métalliques dans un électrolyte de sel en fusion. L'utilisation de cette technologie est prometteuse parce qu'elle offre des possibilités intéressantes d'extraction de tout l'oxygène contenu dans le régolite à des températures plus basses que des processus concurrents qui apparaissent bien moins performants.
Une des clés de la réussite du retour de l'homme sur la Lune et de l'installation de base humaine lunaire, étape préalable à l'exploration de mondes plus lointains, comme Mars est la capacité qu'auront les astronautes de demain à utiliser au mieux les ressources naturelles de façon à les traiter industriellement pour répondre à leurs propres besoins.
Or, l'oxygène liquide est le composant principal de tout carburant de fuséefusée. Il peut représenter jusqu'à 85 % de son poids total. Sa production sur la Lune permettrait ainsi de réduire la massemasse de tout véhicule à destination de la Lune, de réduire hautement les risques techniques afférentsafférents au transport de carburant.
A plus long terme, l'oxygène serait utilisé par les vaisseaux pour se ravitailler en vue de voyages bien plus loin, vers Mars , à la rencontre d'astéroïdesastéroïdes et au-delà, mais d'ici une petite centaine d'années.
Ce qu’il faut
retenir
- Bientôt, des êtres humains partiront pour coloniser la Lune.
- Pour préparer l’expédition, l’Agence spatiale européenne (ESA) a construit une centrale à oxygène du côté des Pays-Bas.
- Objectif : montrer qu’il est possible d’extraire de l’oxygène du régolithe lunaire. Et suffisamment pour subvenir aux besoins des futurs colons.