au sommaire
Alzheimer, Parkinson, quelles cellules pour réparer le cerveau ?
Si les neuronesneurones meurent, pourquoi ne pas les remplacer ? En réalisant des greffesgreffes de neurones fœtaux chez les patients atteints de la maladie de Parkinsonmaladie de Parkinson, cette idée simple s'est révélée remarquablement efficace. La recherche porteporte maintenant sur de nouvelles sources de cellules à greffer, de façon à permettre l'accès au traitement d'un plus grand nombre de personnes.

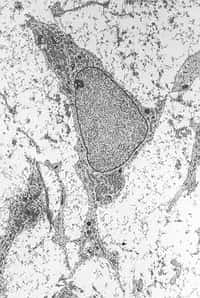
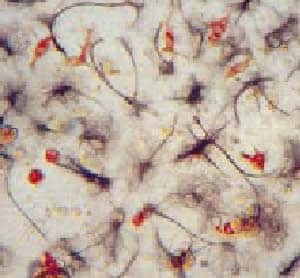
Dans le cadre d'une recherche sur le développement des greffes neuronales pour soigner les maladies de Parkinson et de Hutington, deux équipes suédoise et espagnole ont réalisé des cultures de cellules souches exprimant un gène capable de coder une protéine nécessaire à la production de dopamine (cellules orange). © RDT Info
La mort des neurones, mécanisme du vieillissement
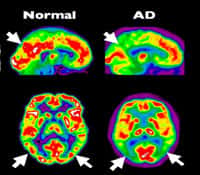
Les neurones meurent, c'est là notre triste destin. Contrairement à d'autres types cellulaires, les neurones morts ne sont pas remplacés. Cette lente diminution fait partie du vieillissement normal de l'organisme. En revanche, la mort neuronale accélérée qui survient dans les maladies neurodégénérativesmaladies neurodégénératives est beaucoup plus handicapante. Elle peut être diffuse, comme dans la maladie d'Alzheimer, ou plus localisée comme dans celle de Parkinson. Dans tous les cas, cette perte a de redoutables conséquences : détérioration cognitive menant à la démencedémence dans le premier cas, troubles moteurs dans le second. Certains médicaments parviennent à ralentir la progression des symptômessymptômes, mais aucune véritable guérisonguérison n'est aujourd'hui envisageable. C'est pourquoi la démonstration que la greffe de nouveaux neurones était capable de corriger les symptômes de la maladie de Parkinson - et d'espérer leur disparition - a été accueillie avec enthousiasme.
La greffe de neurones fœtaux contre Alzheimer
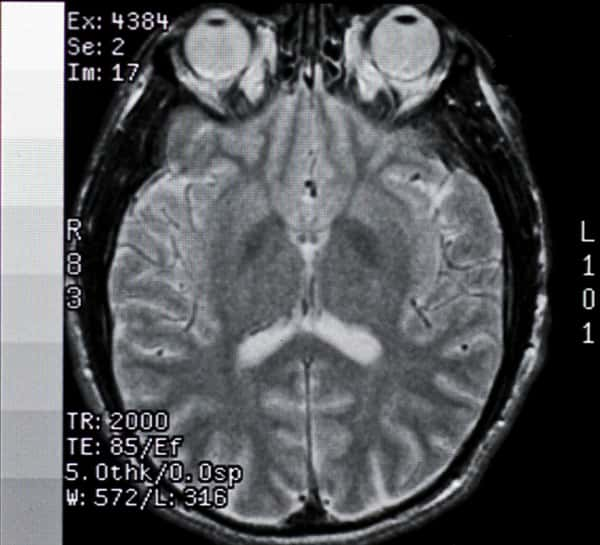
Cette nouvelle thérapiethérapie est née à l'Université de Lund (S), mondialement connue pour ses travaux sur les greffes neuronales, où l'équipe d'Anders Björklund (voir interview) mit au point la greffe de neurones fœtaux chez l'animal, puis son application aux malades de Parkinson. Récemment, un réseau de chercheurs coordonné par Olle Lindvall, de l'Hôpital Universitaire de Lund, a pu établir le bilan positif d'une décennie d'essais cliniquesessais cliniques de cette thérapie chez l'homme. Grâce à l'imagerie cérébrale, ils ont montré que les cellules greffées forment de nouvelles connexions avec les neurones des régions malades et y produisent la substance chimique qui y fait défaut. Ces cellules se révèlent donc capables de réparer le cerveaucerveau !
Très prometteuses, ces thérapies se pratiquent difficilement à grande échelle. Il faut environ six fœtusfœtus, provenant d'avortementsavortements, pour disposer de suffisamment de cellules pour un seul patient. Il est donc impératif de trouver d'autres sources de matériau cellulaire à greffer.
La recherche européenne explore aujourd'hui plusieurs pistes. Un groupe dirigé par Häkan Widner (Wallenberg Neuroscience Center de Lund) a étudié la possibilité de greffer des neurones de porcs et mis au point des moyens de lutter contre leur rejet par le système immunitairesystème immunitaire.
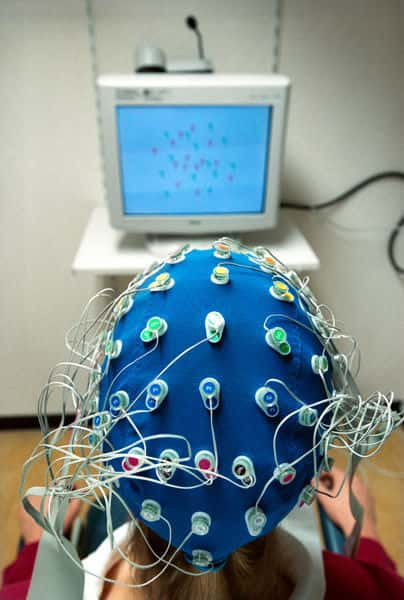
La greffe de neurones fœtaux fonctionne pour réparer les conséquences d'Alzheimer, il faut maintenant trouver d'autres sources de cellules à greffer. © Ars Electronica, Flick CC by nc-nd 2.0
La piste des cellules souches
Une autre voie de recherche porte sur les cellules souches, ces cellules immatures, capables à la fois de se multiplier indéfiniment et de se différencier en tous les types cellulaires du corps humain, présentes spécifiquement dans la moelle osseusemoelle osseuse et la peau. Les scientifiques se penchent avec un intérêt intense sur celles qui existent, semble-t-il, dans le cerveau. Le réseau coordonné par Urban Lendahl (Institut Karolinska, Stockholm) a obtenu des données extrêmement importantes, publiées à deux reprises dans la revue Science, sur l'identification de cellules souchescellules souches neuronales chez la souris adulte et sur la démonstration qu'elles peuvent être la source d'un développement renouvelé de neurones - ce qui représente un espoir pour les maladies neurodégénératives - mais qu'elles ont bien également cette capacité de différenciation en de nombreux autres types cellulaires. Cette multipotence des cellules souches neuronales ouvre ainsi d'immenses perspectives pour de nouvelles voies de reconstruction du corps humain à partir de ses propres éléments.
La médecine régénérativemédecine régénérative suscite l'intérêt de plusieurs jeunes sociétés de biotechnologiebiotechnologie européennes. Deux réseaux de recherche consacrés à la thérapie cellulairethérapie cellulaire du système nerveux sont actuellement financés par l'Union pour associer ces entreprises en plein développement et l'expertise des centres universitaires et hospitaliers. Le premier, coordonné par Marc Peschanski (Inserm U421, Créteil, France), cherche à combiner thérapie cellulaire et thérapie génique en explorant la possibilité de greffer des cellules génétiquement modifiées qui produiront des molécules protégeant les neurones de la mort cellulaire. Le second est dirigé par John Sinden, fondateur, en 1997, de l'entreprise britannique ReNeuron.
« Ce consortium, explique-t-il, vise à trouver des méthodes commercialement viables pour isoler des cellules souches conditionnellement immortalisées et les transplanter dans le cerveau malade. » Au cœur de cette stratégie figure l'utilisation de gènesgènes suicides insérés dans les cellules souches. L'activation à volonté de ces gènes tuerait les cellules greffées, une fois le patient guéri, ce qui permettrait d'éliminer tout risque de transformation tumorale de ces cellules. Une réparation à la carte en quelque sorte...