au sommaire

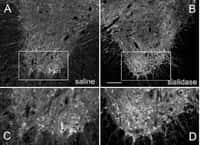
Deux semaines après une blessure médullaire on constate la formation d'une cicatrice qui bloque la repousse axonale, empêchant ainsi la régénération de la moelle épinière.
Jusqu'au début de la deuxième guerre mondiale, le taux de survie des blessés médullaires était inférieur à 5%. Grâce au développement de stratégies d'immobilisation, puis de reconstruction osseuse à partir des années 80, ce taux de survie a été porté au-dessus de 95%. Aujourd'hui, le nombre de blessés médullaires dans le monde est estimé à 2.5 millions, dont 40 % souffrent de tétraplégie (paralysie complète des 4 membres) et 60% de paraplégie (paralysie des membres inférieurs). Parmi ceux-ci, 40% souffrent d'une perte motrice et sensorielle totale. Ces lésions sont permanentes, et les espoirs de récupération après 6 mois quasi inexistants.
Cette absence de récupération a tout d'abord semblé bien mystérieuse : certaines espècesespèces comme le lézard récupèrent spontanément, et les lésions aux nerfs périphériques peuvent guérir même chez notre espèce. La repousse axonale (les axones sont des prolongements des neurones qui permettent la communication à distance) devrait permettre une récupération des fonctions mais elle ne semble pas se faire : pourquoi ? Aujourd'hui, on comprend que le système nerveux centralsystème nerveux central est un milieu non permissif chez l'humain : la repousse axonale y est bloquée par plusieurs facteurs inhibiteurs.
L'identification de certains de ces facteurs a conduit à une explosion des recherches dites de "régénération" ou de "reconstruction" de la moelle épinièremoelle épinière. Il faut néanmoins comprendre qu'il ne s'agit pas de réparer des lésions anciennes, mais plutôt de rendre le milieu permissif à une récupération spontanée. La distinction est d'importance : cela signifie que, en l'état de nos connaissances, ces approches ne peuvent pas s'appliquer à des lésions anciennes. La limite théorique est de 6 mois, mais la diminution rapide du potentiel de régénération suggère que des interventions dans les jours ou les premières semaines suivant la blessure seraient préférables.
Malgré cette limitation importante, trouver un traitement pour les nouveaux cas de blessures médullaires serait évidemment fantastique. Les recherches actuelles portent principalement sur les approches suivantes :
- limiter les dégâts : lors d'une lésion, seule une petite partie des neurones va réellement mourir sur le coup. La plupart des dommages vont arriver dans un deuxième temps, en partie à cause de la toxicitétoxicité des composants dispersés lors de la mort cellulaire primaire. Plusieurs moléculesmolécules permettent de limiter ces dommages secondaires, et la recherche de nouvelles molécules continue. Il est vraisemblable que les progrès les plus rapides viendront de cette approche, qui cible également les accidentsaccidents vasculaires cérébraux.
- attaquer les facteurs inhibiteurs : plusieurs approches tentent de supprimer les facteurs inhibiteurs intrinsèques à la moelle épinière (Nogo-A, MAG, OMgp, etc.) ou exprimés dans la cicatricecicatrice en formation (CSPG, Ephrin-A5A5, Ephrin-B3, EphA4, etc.). Certaines approches tentent d'attaquer ces protéinesprotéines par des anticorpsanticorps, voire de vacciner un organisme contre ses propres protéines. D'autres tentent de bloquer l'action de ces facteurs en supprimant leurs effets métaboliques (via les rho-GTPasesGTPases) au niveau des axones en voie de régénération. Certains résultats sont prometteurs chez l'animal, mais le transfert à l'humain semble particulièrement difficile avec ces approches. La multitude de substances impliquées suggère que beaucoup de travail reste à faire pour comprendre les mécanismes activés lors d'une blessure.
- stimuler et guider la repousse axonale : plusieurs molécules (BDNF, NT3, GDNF, etc.) sont connues pour améliorer ou guider la repousse des axones. Après une période d'optimisme, il est apparu que ces facteurs neurotrophiques ne suffisent pas à contrer le caractère inhibiteur du milieu et présentent quelques effets secondaires négatifs (notamment une augmentation de la mort neuronale) qu'il faut compenser par ailleurs. Plus ennuyeux, il semble difficile d'assurer que la repousse axonale soit sélective, c'est-à-dire sur les bonnes cibles.
- ponter la blessure : la lésion médullaire induit une cicatrice qui représente une barrière physiquephysique difficile à franchir. Plusieurs approches tentent de supprimer ce problème en pontant la blessure avec des substratssubstrats synthétiques, des portions de nerf périphériques (cellules de Schwanncellules de Schwann), voire des fibroblastesfibroblastes génétiquement modifiés pour exprimer des facteurs neurotrophiques. Dans cette optique, une des techniques les plus intéressantes passe par l'utilisation de cellules glialescellules gliales particulières : les OEG (Olfactory Ensheating Glia). Ces cellules se retrouvent au niveau du système olfactif, lequel a une particularité unique dans le système nerveux central : permettre des régénérations ! Tout porteporte à croire que cette particularité est due aux OEG, qui semblent protéger et guider les axones en voie de régénération. Plus étonnant encore, certaines données suggèrent que ces OEG sont capables de sélectivité, c'est-à-dire d'amener les axones vers leur cible d'origine. Des résultats impressionnants ont été obtenus chez le rat par cette approche, que rien a priori n'empêche de combiner avec les autres.
Ainsi, plusieurs expériences de régénération de la moelle épinière ont abouti à des résultats parfois spectaculaires chez l'animal. L'espoir est permis qu'un jour, les blessures médullaires n'entraîneront plus automatiquement des handicaps majeurs. Le passage de l'animal à l'humain n'est toutefois jamais garanti, et les premières thérapiesthérapies efficaces ne verront vraisemblablement pas le jour avant de (trop) nombreuses années.
Pour en savoir plus, la référence suivante inclut (en plus d'une revue qui a inspiré le présent article) une liste de liens pointant une trentaine de projets en cours, en spécifiant l'approche étudiée et le stade d'avancement des travaux : Schwab M, Brechtel K, Mueller CA, Failli V, Kaps HPHP, Tuli SK, Schluesener HJ (2006) Experimental strategies to promote spinal cord regeneration--an integrative perspective. Progress in Neurobiology (sous presse).