La curcumine, que l’on retrouve dans le curcuma, ou safran des Indes, pourrait empêcher l’agglutination de l’alpha-synucléine, une des premières étapes de la maladie de Parkinson. Alors doit-on prescrire un régime alimentaire plus épicé aux patients ? Malheureusement non, cela ne suffira pas. Mais une nouvelle voie est ouverte.
au sommaire

La curcumine, extraite du curcuma, se retrouve dans l'alimentation puisqu'elle est utilisée en tant que colorant jaune, avec la référence E100. En plus d'empêcher la formation d'agrégats d'alpha-synucléine dans la maladie de Parkinson, la curcumine a des propriétés antiseptiques et anti-inflammatoires. © Sanjay Acharia, Wikipédia, cc by sa 3.0
- À lire, notre dossier sur la maladie de Parkinson
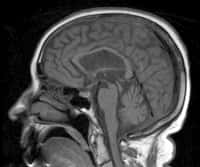
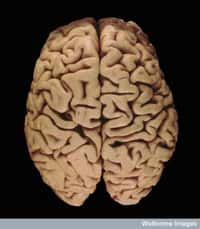
Dans le calendrier international, le 12 avril coïncide avec la Journée mondiale de la maladie de Parkinson. Cette pathologie neurodégénérative, relativement courante chez les personnes âgées (près de 5 % des adultes de plus de 80 ans), se caractérise par un déficit du système dopaminergique, et de la présence de corps de Lewy, des agrégats anormaux de protéines dans les neurones, dont le principal constituant est l'alpha-synucléine.
Cette moléculemolécule, en s'agglutinant, a déjà été directement incriminée dans les premières étapes de la maladie de Parkinson. L'un des objectifs des scientifiques consiste à prévenir cette agglomération caractéristique, si possible avant qu'elle ne se produise. Et comme la nature est bien faite, la réponse pourrait venir des plantes. Plus précisément du curcuma, autrefois appelé safran des Indes, dont on utilise le rhizomerhizome pour composer de nombreuses épices.
Parmi ses composés, une molécule appelée curcuminecurcumine, déjà connue pour ses propriétés antioxydantes. Mais son pouvoir thérapeutique ne se limiterait pas à cela. D'après une étude publiée dans le Journal of Biological Chemistry, ce principe actifprincipe actif est doté d'une forte affinité pour l'alpha-synucléine, et la liaison entre les deux molécules empêcherait la protéine de s'agglutiner dans les neurones.
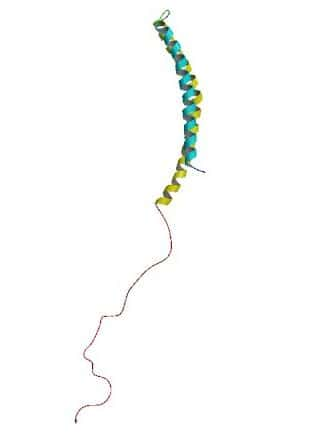
La curcumine remet en forme l’alpha-synucléine
S'il est assez facile de connaître la suite d'acides aminésacides aminés qui composent une protéine, comprendre la façon dont ils s'agencent entre eux pour donner une forme globale et tridimensionnelle à la molécule est une autre performance. D'autant plus que l'on a cru durant longtemps que l'alpha-synucléine était une protéine intrinsèquement désordonnée, c'est-à-dire sans structure 3D stable...
Dans cette étude, les chercheurs de l'université d’État du Michigan (États-Unis) se sont focalisés sur le repliement dans l'espace de l'alpha-synucléine. Or, en présence de curcumine, d'autant plus quand on élève les températures, la protéine adopte bien plus rapidement une structure en tétramère qui la stabilise et diminue sa tendance à s'agglomérer avec d'autres peptidespeptides. En ne laissant que très peu de temps l'alpha-synucléine sous sa forme toxique, la curcumine prévient alors la formation d'agrégats mortels dans les neurones.
Alors, faut-il manger épicé pour en finir avec la maladie de Parkinsonmaladie de Parkinson ? Le problème est bien plus compliqué. Sous cette forme, la curcumine ne franchit pas la barrière hématoencéphalique (qui protège le cerveau de pathogènespathogènes, de toxinestoxines... mais aussi de certains principes actifs) et ne peut cibler in vivoin vivo l'alpha-synucléine. Les chercheurs proposent plutôt de trouver des médicaments dotés des mêmes propriétés thérapeutiques pour reconfigurer les protéines défaillantes. Mais même si un tel traitement voyait le jour, suffirait-il à soigner tous les symptômessymptômes de cette maladie multifactorielle ? Probablement que pour la maladie de Parkinson, le remède miracle et universel n'existe pas...