au sommaire
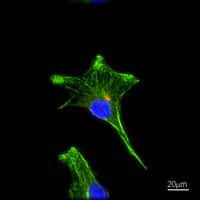
Un cardiomyocyte, une cellule du muscle cardiaque, que l'on a longtemps cru incapable de se diviser et qui y parvient pourtant, parfois. © R. Bick, B. Poindexter, UT Medical School / Science Photo Library
On savait déjà que, même chez les mammifèresmammifères, le cœur présente une certaine capacité de régénération, contrairement à ce que l'on a longtemps pensé. En 2001, chez la souris, une équipe américaine avait observé que des nouvelles cellules apparaissaient au niveau de lésions cardiaques, comme lors d'une cicatrisation. Récemment, une équipe américaine a découvert des cellules souches à l'intérieur même du muscle cardiaque, capables de se différencier pour se transformer en d'autres types cellulaires présents dans le cœur.
Installer de telles cellules souches au niveau d'une lésion cardiaque semble donc une possibilité thérapeutique pour obtenir une forme de cicatrisation. Mais une autre voie semble possible : celle de stimuler la - faible - capacité des cellules du muscle cardiaquemuscle cardiaque (les cardiomyocytes) à se diviser pour se multiplier. Seules quelques-unes tentent l'aventure - 0,6% - et, parmi elles, très peu (un huitième) y parviennent.
C'est cette voie qu'explorent Bernhard Kühn et ses collègues (Children's Hospital and Harvard Medical School, Boston). En 2007, ces chercheurs avaient pu stimuler la division des cardiomyocytes chez le rat à l'aide d'un patch (en matièrematière spongieuse) imprégné de périostine, un dérivé de la paroi osseuse, que l'on trouve en abondance dans les tissus du fœtus ou, chez l'adulte, dans un muscle blessé, mais qui reste très rare dans le cœur. Cette technique en est aujourd'hui aux tests précliniques à l'Hôpital des enfants malades de Boston.
La même équipe vient aujourd'hui d'aller un peu plus loin. Après avoir provoqué des crises cardiaques chez des souris, les chercheurs ont injecté aux animaux une protéine, la neuréguline-1, NRG1. Bien connue, cette moléculemolécule joue le rôle, chez le fœtus, de facteur de croissancefacteur de croissance du système nerveux (d'où son nom) mais aussi du muscle cardiaque.
Une belle voie ouverte... mais qui reste à explorer en détail
Après douze semaines de traitement et deux semaines d'attente (pour éliminer les effets directs de la NRG1, expliquent les auteurs de l'étude), les cœurs des souris traitées présentaient des cicatricescicatrices 46% plus petites que chez les animaux non traités. De plus, le cœur se remet bien mieux et la puissance de la pompe cardiaque semble plus grande.
Tentant de comprendre les mécanismes à l'œuvre, l'équipe, lors d'une autre expérience, a étudié l'effet de la stimulationstimulation d'un récepteur de la NRG1, ErbB4. Là aussi, il en est résulté une prolifération inhabituelle de cardiomyocytes. Sur le plan médical, l'observation a de quoi alerter les scientifiques. Un médicament utilisé contre le cancer du seincancer du sein, l'herceptine (un anticorpsanticorps monoclonalmonoclonal), agit justement en inhibant un récepteur semblable au ErbB4 et certaines femmes traitées avec cette molécule développent des malformationsmalformations cardiaques. S'il existe un lien entre l'activité de ce récepteur et le développement de tumeurstumeurs, la prudence s'impose...
Les chercheurs ont aussi découvert que la NRG1 agit préférentiellement sur les cardiomyocytes à un seul noyau. Il en existe en effet qui en possèdent plusieurs. Il reste à comprendre mieux cette sélectivité, d'autant que la proportion de cardiomyocytes à un seul noyau varie beaucoup d'une espèceespèce à l'autre. L'effet chez un être humain adulte pourrait être passablement différent de ce que l'on observe chez la souris.
Le chemin qui mènerait à une applicationapplication thérapeutique risque donc d'être long mais les auteurs de l'étude soulignent l'intérêt d'un tel procédé, consistant à stimuler la prolifération des propres cellules du patient, en comparaison de la méthode - toujours hypothétique elle aussi - des cellules souchescellules souches implantées, beaucoup plus invasive.