au sommaire
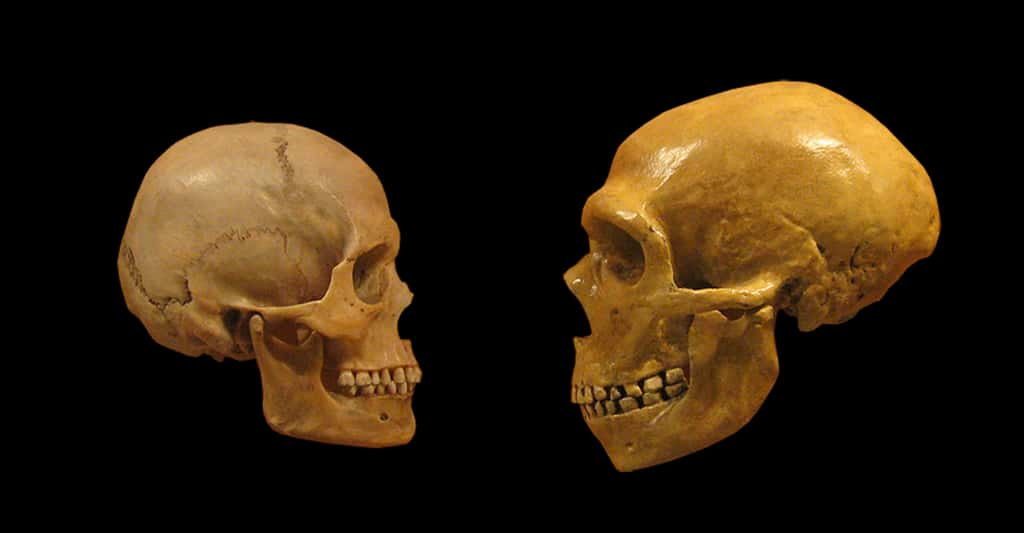
Les isotopes radioactifs sont des acteurs naturels de la mesure du temps. Des appareils reposant sur l'analyse de leur désintégration permettent de calculer l'âge d'une roche.
Nous avons tous entendu parler de la méthode du carbone 14 (on l'écrit 14C). Le chiffre 14 est le nombre de masse de ce carbone, ce qui veut dire qu'il existe d'autres « carbones », avec des nombres de masse 12 et 13.

Grâce à un spectromètre de masse, il est possible de calculer l'âge d'une roche. © Wpcm
Tous ces « carbones » ont quasiment les mêmes propriétés chimiques, tout simplement parce qu'ils ont le même nombre d'électrons autour de leur noyau, ce qui leur donne d'ailleurs le nom de carbone. En revanche, ils ont une masse différente : ce sont les isotopes du carbone.
La désintégration des isotopes radioactifs
Certains de ces isotopes sont stables alors que d'autres disparaissent en se transformant en d'autres isotopes de façon naturelle au cours du temps : on dit qu'ils se désintègrent et qu'ils sont radioactifs. Ainsi, le carbone 14 se transforme en azote 14. Notons que cette transformation est majeure, puisqu'ici un solidesolide se transforme en gazgaz !
Cette transformation est extrêmement énergétique car elle affecte le noyau de l'atomeatome, ce qui explique pourquoi ce phénomène radioactif peut être utilisé pour fabriquer de l'énergieénergie ou des armes dites « nucléaires ».
La radioactivité est un phénomène physique naturellement présent dans l'univers. Elle est due à des noyaux atomiques instables qui se désintègrent et dégagent des rayonnements divers plus ou moins pathogènes. Unisciel et l’université de Lille 1 nous éclairent, avec le programme Kézako, sur les risques et les effets de ces rayonnements. © Unisciel
La nature est d'une sophistication dont on n'a encore perçu qu'une infime partie, mais l'Homme sait y déceler ce qui peut lui servir, pour le meilleur et pour le pire. Pour notre affaire, ces transformations, ou désintégrations, s'effectuent statistiquement sur un très grand nombre d'isotopes de manière si régulière que l'on peut s'en servir d'horloge.
La comparaison classique est celle du sablier qui laisse passer les grains de sablesable à débitdébit constant lorsque les grains sont suffisamment nombreux.

L'Homme peut se servir de la désintégration des isotopes radioactifs pour calculer l'âge d'une roche, un peu comme un sablier mesure le temps. © DR
Calculer l'âge d'une roche
Entendons-nous bien, nous désirons ici savoir depuis combien de temps une roche s'est formée. Par exemple : quand une coulée de lavelave s'est-elle solidifiée ? Un chronomètrechronomètre se définit par la transformation d'un isotope père (P) en un isotope fils (F). (Voir schéma ci-dessous).
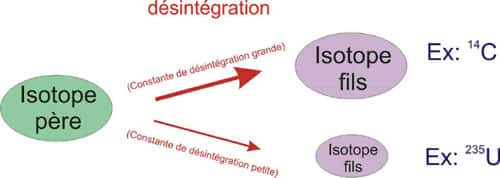
À chaque problème géologique son chronomètre. © DR
L'âge calculé au temps t, aujourd'hui, pendant la mesure, ne dépendra que de deux facteurs :
- le nombre d'isotopes pères à l'instant zéro (P0) ;
- Un facteur λ (= constante de désintégration de l'isotope) qui caractérise la « vitessevitesse » de désintégration d'un isotope-père donné (c'est-à-dire le diamètre du trou du sablier par rapport au diamètre des grains de sable).
Problème : on ne connaît pas P0 mais seulement le nombre d'atomes pères actuels (Pt), c'est-à-dire restants. On s'en sort très bien en mesurant le nombre d'atomes fils (F) et Pt car
Remarque : à chaque problème géologique son chronomètre :
- Si on fait de l'archéologie, on va travailler dans des périodes très récentes pour le géologuegéologue, de quelques centaines ou milliers d'années, et on va donc utiliser un chronomètre « rapide » : le 14C, à grande constante de désintégration λ (voir schéma ci-dessus).
- En revanche, si on s'intéresse à l'apparition de la vie sur Terre, on va travailler à l'échelle du milliard d'années et il nous faudra alors un chronomètre « lent » permettant l'accès au père restant encore abondant : on utilisera alors les méthodes uraniumuranium/|bcb4a0bce920e80eac294b76f0826b6f| |529ea36df8dac6cdc8b398ef2638fdaf|/strontiumstrontium ou samariumsamarium/|d0d6b7c8351282ea9770cd47fe939332| par exemple (Roth et Pothy, 1985).
Deux types de mesures peuvent être faites avec différentes machines.
Spectromètre de masse
Il est possible de mesurer directement dans une roche ou un minéralminéral le nombre d'isotopes pères (Pt) et d'isotopes fils (F). Pour cela, nous devons utiliser un appareil qui permet de séparer les isotopes d'un même élément, en utilisant ce qui les distingue, c'est-à-dire leur masse.

Comment fonctionne un spectromètre de masse ? © DR
Cela se fait grâce à un spectromètrespectromètre de masse (voir photo et schéma ci-dessus), un appareil très simple dans son principe mais très sophistiqué au niveau de la précision de la mécanique et de la stabilité électronique :
- Une source d'ionsions envoie un faisceau focalisé qui entre dans le champ magnétiquechamp magnétique d'un électro-aimantaimant.
- Celui-ci dévie la trajectoire de chaque isotope en fonction de sa masse ; c'est donc lui qui sépare les différents isotopes les uns des autres.
- Chaque faisceau individuel est ensuite focalisé sur un détecteur qui mesure soit les ions individuellement, soit un courant, très faible, qui devra être fortement amplifié.
Ces appareils, très onéreux, sont utilisés pour l'utilisation des méthodes de datation classiques telles que uranium/plomb, rubidium/strontium, potassiumpotassium/|cc09454badaaba4940f0b78ecebf95ac| etc.
Compteurs alpha, gamma ou bêta
Deuxième cas : on ne mesure pas directement le nombre d'isotopes de la roche, mais on compte les désintégrations individuelles de chaque isotope. En effet, à chaque désintégration se libère une particule de l'atome qui émet une énergie spécifique à l'isotope que l'on mesure.
En fonction du type de particule émise, on utilise un compteur alpha, gamma ou bêta (nom des particules émises). Cet appareillage est utilisé dans le cas des méthodes géochronologiques du plomb 210, de l'uranium/thoriumthorium, des isotopes du radiumradium, etc.