au sommaire
La croissance d'un cristal obéit à des lois précises et dans des conditions de pression et de température spécifiques. L'industrie, quant à elle, utilise différents procédés pour la croissance artificielle.

Les conditions de croissance
La croissance se fait par accrétion, en suivant la maille élémentaire du cristal à partir du germegerme de croissance qui peut être une impureté ou un minuscule cristal de la même espèceespèce qui ne mesure que quelques angströms (1Å=10-10 m), composé d'au moins 200 atomes et qui possède en lui une forme similaire à celle du futur cristal, ou encore à partir d'une mince tranche de cristal suspendue à un crochet dans le cas des synthèses.
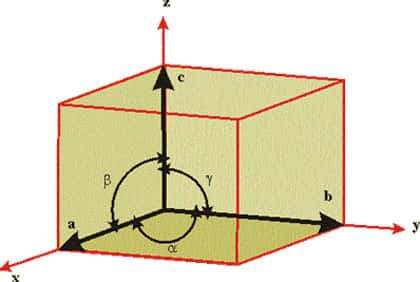
La croissance d'un cristal se fait selon des lois précises à partir de la solution mère dont le solvant est de l'eau, et dans des conditions de pression et de température spécifiques. Si on utilise, dans le cas des synthèses artificielles un autre solvant que l'eau, on parlera de croissance de flux pour le cristal fabriqué. Le flux est donc n'importe quel autre liquide que l'eau utilisé pour la fabrication d'un cristal, par opposition à la formation hydrothermale classique du minéralminéral.
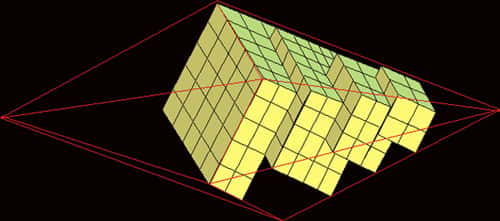
Rappel de quelques lois de la cristallographie.
- Loi de la constance des angles de Sténon et Romé de Lisle. « Dans une même espèce cristalline, l'angle dièdre de faces correspondantes est constant. » De cette façon, un monocristal croissant formera toujours un polyèdre convexeconvexe limité par des faces planes, c'est-à-dire que dans des conditions optimales, il ne se formera jamais aucune forme arrondie dans un cristal, de même que les faces du cristal sont parallèles 2 à 2 avec celles du cristal originel.
- Loi de stratificationstratification multiple d'Haüy. « Un cristal d'une même espèce est constitué, quel que soit son facièsfaciès, par la juxtaposition de parallélépipèdes élémentaires, tous identiques entre eux et caractéristiques de l'espèce. »

- Loi de Curie. « Un corps tend à prendre la forme qui présente une énergieénergie superficielle minimum compatible avec les forces d'orientationforces d'orientation. Ce minimum d'énergie potentielleénergie potentielle de surface introduit comme solution pour un volumevolume donné celle qui fournit la surface minimum compatible avec les liaisons. » Ce principe de minimisation de l'énergie pour tendre vers une position d'équilibre est universel. Il est également applicable à la situation des atomes, ionsions et moléculesmolécules au sein même du cristal, en particulier pour l'énergie réticulaire de cohésion du cristal.
Quand on trouve un cristal brut, mettons un diamantdiamant ! On peut voir à sa surface des couches superposées et de plus en plus petites en superficie qui traduisent la croissance du cristal. Ceci peut aussi indiquer que le cristal a partiellement refondu puisque le processus de fontefonte va se faire exactement à l'inverse de celui de la croissance et en suivant les mêmes contraintes géométriques. Il arrive que l'on puisse voir ces couches à l'intérieur d'un cristal.
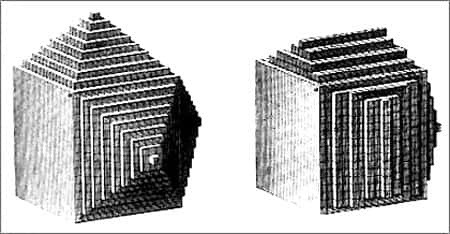
La neige, un cas particulier
La naissance d'un flocon de neige dépend de la vapeur d'eau, la température et... la poussière. La vapeur d'eau doit être suffisamment dense pour qu'elle s'y condense à la première occasion, sous forme de glace, si la température est inférieure à 0 °C. La saturation dépend de la température : elle est atteinte pour 5 g/m3 à 0 degré et 1 g/m3 à -18 °C. Quand l'atmosphèreatmosphère est très propre, les germes sont rares. La densité de vapeur d'eau peut dépasser quatre fois la valeur de saturation sans que la moindre glace ne se forme.
À un certain niveau de sursaturation, toutefois, les chocs entre molécules d'eau finissent par créer des agrégats assez volumineux. Dans les nuagesnuages de neige, la croissance de la glacecroissance de la glace s'amorce à la surface de poussières. Ces poussières sont, par exemple, de mica ou d'argileargile ou de sel, excellents germes de croissance, car leur surface est faite d'atomes d'oxygèneoxygène arrangés suivant une structure proche de celle de la glace. Des particules de 1/100e de millimètres se couvrent de glace dès que la saturation est atteinte. En revanche, les poussières submicrométriques que l'on trouve au-dessus de 4.000 mètres d'altitude ne servent de germes que si l'atmosphère est sursaturée. Si le rapport surface/volume est assez grand, la croissance est possible. Les impuretés permettent d'atteindre cette taille critique.

Pour la glace, il se forme autour des germes des cristaux prismatiques hexagonaux. Les cristaux plus compliqués sont issus de l'évolution de ces cristaux simples, d'où une symétrie hexagonale. Les angles du cristal de départ donnent naissance à des branches. La formation de cristaux dendritiques est alors favorisée. Le cristal initial de glace est de forme vaguement sphérique même si sa surface est très irrégulière à l'échelle moléculaire. La croissance réduit très rapidement cette rugosité, les molécules d'eau se fixant préférentiellement là où elles peuvent établir le plus de liaisons avec leurs semblables, donc dans les creux. Petit à petit, la croissance engendre des plans cristallins. Le cristal est un prisme hexagonal, dont les faces supérieure et inférieure sont des hexagones (angles de 120 et 60 degrés) et les faces des rectangles. Dans l'étape suivante, la nature de la surface de la glace joue un rôle dominant.
Les molécules de surface forment une couche, quasi liquide qui n'existe pas quand il fait très froid. Puisque la surface du cristal est quasi liquide, les molécules qui s'y déposent, peuvent s'y déplacer ensuite jusqu'à l'endroit le plus favorable (un creux !) avant de se fixer. Selon la température, ce processus de diffusiondiffusion est plus ou moins lent, ce qui affecte la forme prise par le flocon. Ainsi, selon les conditions atmosphériques, les flocons, jusque-là tous jumeaux, adoptent une multitude de formes.
Trois modes de croissance dominent. Les deux premiers sont commandés par la température. Selon la valeur de celle-ci, ce sont soit les faces hexagonales, soit les facettes latérales, qui « poussent » le plus vite. Entre -10 °C et -5 °C, les bases hexagonales se développent plus : à -6 °C par exemple, cette vitessevitesse de croissance est le double de celles des facettes latérales et le flocon a alors l'aspect d'une colonne. Aux températures supérieures à -5 °C ou inférieures à -10 °C en revanche, les facettes croissent plus rapidement que les faces hexagonales : elles poussent par exemple de 0,5 millième de millimètre par seconde à -13 °C, soit quatre fois plus que ne le font les bases. Un flocon de neige qui reste à cette température pendant toute sa croissance prend la forme d'une plaquetteplaquette hexagonale.

Le troisième mode de croissance est commandé par la concentration en eau de l'atmosphère où se forme le flocon. Plus la sursaturation est importante et plus le cristal croît vite. Lorsque la vitesse de croissance devient trop grande ou quand le cristal est devenu grand, les molécules d'eau qui se déposent n'ont guère le temps de migrer à la surface cristalline avant de se fixer. Il en est de même à très basse température lorsque la couche quasi liquide est absente. Les molécules d'eau se fixent près de l'endroit où elles ont rencontré la surface cristalline : les arêtes, et plus les arêtes croissent, plus elles font saillie, et plus leur croissance s'accélère. C'est par ce mécanisme que se forment les flocons en forme d'étoilesétoiles à six branches.
Le même mécanisme fonctionne aussi de façon plus compliquée. Ainsi, il arrive que les branches à leur tour se dentellent, se subdivisant en branches plus petites, qui elles-mêmes se divisent... L'origine de cette magnifique ramification et de sa régularité a été expliquée en 1964 par les Américains Mullins et Sekerka, qui s'intéressaient aux nombreuses structures ramifiées observées en métallurgie. Mullins et Sekerka ont montré qu'une surface plane qui croît trop vite se couvre de bosses séparées par une distance d'autant plus petite que la vitesse de croissance est grande. Dans le cas du flocon, la subdivision des branches d'un flocon n'intervient que si la vitesse de croissance est assez grande pour que la longueur séparant deux nouvelles aiguilles (les bosses) soit inférieure à la longueur des aiguilles déjà constituées.
La croissance artificielle
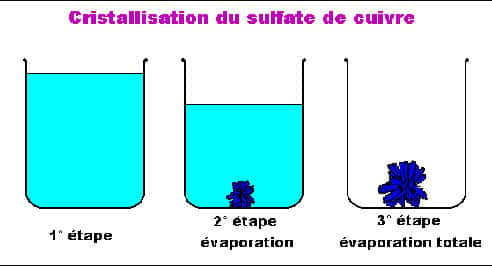
Une petite expérience : la cristallisation du sulfate de cuivrecuivre. Prenons un récipient transparent contenant une solution de sulfate de cuivre assez concentrée (bouillie bordelaisebouillie bordelaise des jardiniers !). On laisse l'eau s'évaporer, pendant plusieurs semaines si nécessaire sans bouger le récipient et il restera, dans le fond du récipient, de beaux cristaux de sulfate de cuivre ! La solution (celle de sulfate) était saturée, et lorsque le solvant (l'eau) a commencé à s'évaporer, le sulfate s'est déposé dans le fond du bécherbécher. Plus la duréedurée de cristallisation est longue, plus gros sont les cristaux.
Notons les principaux procédés artificiels industriels.
- Procédé Verneuil : on fait fondre de la poudre d'aluminealumine sur une amorce située dans la zone de cristallisation. Par adjonction de divers oxydes de métauxmétaux, on obtient différentes couleurscouleurs (Mn, Co, Cr, Cu, Fe, Ti). Il existe des corindons de synthèse étoilés. Ces pierres sont tellement belles, qu'elles sont suspectes pour l'analyste.
- Procédé par tirage (Czochralski) : une amorce de corindon naturel est trempée dans « une soupe » chauffée à ± 2.440 °C dans un four en iridiumiridium. Types de pierre : rubis, rubis étoilés ainsi que des corindons orange.

- Procédé par fonte zonale (Seiko) : procédé sans creuset. Une poudre d'aluminiumaluminium est fondue zonalement et lentement afin d'obtenir un cristal longitudinal unique. Rubis et corindons orange.
- Procédé anhydre (procédé fusionfusion liquide - méthode flux) : la plupart des corindons synthétiques sont produits par ce type de procédé. Dans un creuset à parois de platineplatine, on mélange de la poudre d'oxyde d'aluminium pure avec des oxydes métalliques (colorants) entre 900 °C et 1.400 °C pendant un temps assez long. Le refroidissement se faisant lentement (± 2 °C par heure), des cristaux se forment en conglomératconglomérat. Un système complexe de variation de température est appliqué en vue de permettre l'obtention de cristaux plus importants.
La recherche et l'industrie
Les matériaux monocristallins massifs sont utilisés dans de nombreux dispositifs industriels en électronique, en optique et en optoélectroniqueoptoélectronique. La maîtrise des outils et des conditions de croissance cristallinecroissance cristalline s'avère primordiale pour l'obtention de cristaux de grande pureté et de haute qualité cristalline répondant aux critères recherchés.
Les secteurs d'activité : chimiechimie, pharmacie, commerce, électronique, robotiquerobotique... Par exemple : scintillateur, piezoélectrique, laserlaser, semi-conducteursemi-conducteur, scintillateurs pour la détection de rayonnements, monochromateurs, vision nocturnenocturne, etc.
Le film de diamants CVD… Une technologie d'avant-garde
Le Laboratoire de science et génie des surfaces est une Unité mixte de recherche associée au CNRS (UMR 7570). Il est situé dans une école d'ingénieurs (École des Mines de Nancy) et dans un environnement d'Écoles d'ingénieurs de l'Institut national polytechnique de Lorraine. (Nos remerciements à ce laboratoire pour nous avoir autorisé à utiliser ses images et sa collaboration dans ce dossier).
Les propriétés exceptionnelles du diamant incitent à des applicationsapplications potentielles en tant que céramiquecéramique. Leur développement dans le domaine de la mécanique, limité par le coût du diamant naturel, a pu se faire grâce à l'élaboration du diamant dans des conditions de stabilité thermodynamiquethermodynamique (hautes températures et hautes pressions). Les limites de ce procédé, la faible taille des cristaux, l'impossibilité d'obtenir des films, n'ont pas permis le développement d'applications thermiques, optiques et électroniques.
La possibilité de synthétiser du diamant dans des conditions métastablesmétastables, à partir de 1960, a relancé l'intérêt pour l'élaboration du diamant, et en particulier la formation de films. Ces techniques utilisent le dépôt chimique en phase vapeur (techniques CVD).
Pour exploiter les propriétés du diamant telles que transparencetransparence optique, conductivité thermiqueconductivité thermique, caractère semi-conducteur extrinsèque, l'obtention de films pratiquement monocristallins sur substratssubstrats non-diamant (siliciumsilicium) est un objectif majeur. Les dépôts sont élaborés sur du silicium monocristallin, puis caractérisés par microscopies électroniques, par spectrométriespectrométrie Raman ou par diffractiondiffraction X.

Le choix d'élaborer du diamant par dépôt chimique en phase vapeur assisté par plasma micro-onde est lié à la formation d'un plasma froid hautement énergétique. Le procédé consiste à plonger un échantillon dont la nature et l'état de surface sont contrôlés, dans une décharge luminescente constituant un milieu (hors équilibre thermodynamique) favorable à la formation de la phase diamant. Cette décharge est obtenue par excitation micro-onde d'un gazgaz plasmagène contenant le carbonecarbone nécessaire à la synthèse (gaz vecteur CH4), dilué dans de l'hydrogènehydrogène. Lorsque la surface du substrat est convenablement préparée et est soumise à la décharge à une température comprise entre 600 °C et 900 °C et sous une pression de l'ordre de 10 à 50 hPa, la phase diamant germe sous la forme de petits cristaux facettés. Ceux-ci croissent puis se rejoignent (étape de coalescencecoalescence) pour former un film continu polycristallin. Ce film peut ensuite s'épaissir si la synthèse se poursuit.

Pour favoriser la germination et la croissance de cristaux de diamant aux dépens du graphitegraphite (phase stable), la décharge micro-onde doit être particulièrement réactive et contenir des espèces actives telles que des radicaux libresradicaux libres, des ions et des électronsélectrons énergétiques (la température équivalente de ces électrons atteint 104 K). Il est important de créer une décharge parfaitement homogène interagissant avec la totalité de la surface à revêtir. L'étude des conditions de température, de pression et de composition gazeuse permet la synthèse de cristaux de bonne qualité se prêtant à la formation de films continus. La morphologiemorphologie de ces cristallites (variant du cube à l'octaèdre selon les conditions) conditionne ensuite la qualité microstructurale des films avec, en particulier, la formation de texture cristallinetexture cristalline.

La création de défauts structuraux est particulièrement rédhibitoire à la réalisation de films diamant potentiellement utilisables dans des applications optiques ou électroniques. La maîtrise de la texture des films polycristallins permet de minimiser la formation de ces défauts en privilégiant la croissance du diamant selon certaines de ces faces cristallinesfaces cristallines moins enclines à former ces défauts.

Une étape supplémentaire dans la qualité des films diamant est l'élaboration de films hétéroépitaxiés où les cristaux germent en relation d'orientation avec le substrat de silicium. Ces relations d'orientation entre les cristallites et le substrat ne sont observées que lorsqu'un prétraitement particulier du silicium est réalisé in situ. Celui-ci consiste à polariser négativement le substrat par rapport à une anodeanode plongée dans la décharge micro-onde. Cette polarisation conduit à la formation d'une seconde décharge (appelée décharge diode) qui se superpose à la décharge micro-onde. La complexité du processus de germination du diamant sous polarisation (prétraitement appelé BEN pour Bias Enhanced Nucleation) est liée à la présence simultanée de deux plasmas (micro-onde et diode) qui agissent sur la surface du silicium de façon concertée, est mal connue.
Les études actuelles portent sur la compréhension des mécanismes de germination et les interactions entre cristaux et substrat dans les premiers instants de la synthèse sous l'effet du plasma diode de polarisation. La microscopie électronique à balayage haute résolutionrésolution (HR-MEBMEB) permet une caractérisation précise des premiers stades de formation des cristaux de diamant en termes de taux de recouvrement, de densité de cristaux, de taille moyenne des particules et de taux d'épitaxie (pourcentage de cristaux en épitaxie avec le silicium). La croissance de tels revêtements conduit à la formation de films hautement orientés (voir figure ci-dessus) où la densité de défauts diminue fortement et où l'on s'approche de la synthèse d'un film monocristallin dont les propriétés tendent vers celles d'un diamant naturel.