au sommaire
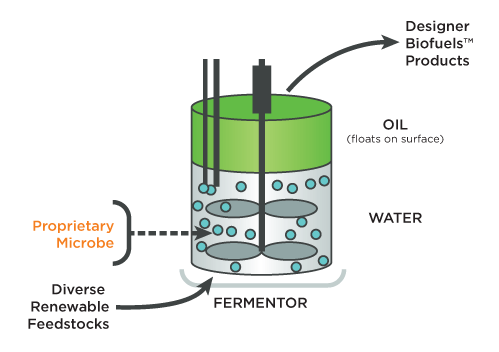
Une fois synthétisé, le biodiesel produit par les bactéries est libéré dans l'environnement aqueux et remonte vers la surface. Il ne reste plus qu'à l'aspirer. © LS9
Les biocarburants représentent probablement l'avenir de notre société de consommation. De nombreux laboratoires de recherche et entreprises l'ont bien compris. Les défis à relever ne manquent pas, mais leur nombre diminue progressivement au cours du temps. Pour éviter toute compétition avec l'agriculture alimentaire, et donc produire des agrocarburantsagrocarburants de deuxième génération, des spécialistes essaient d'exploiter des réactifsréactifs tels que les déchets végétaux. Jay Kiesling, cofondateur de la société LS9 et chercheur de l'université de Californie à Berkeley, a par exemple créé en 2010 une bactériebactérie Escherichia coliEscherichia coli (souche A2A) capable de convertir la cellulosecellulose en biodiesel.
Dans un premier temps, le polymèrepolymère est dégradé en sucressucres grâce à la libération exogèneexogène d'hémicellulase. Ceux-ci sont ensuite absorbés et transformés en sous-produits, acide grasacide gras et éthanol, puis en estersesters méthyliques d'acide gras à longue chaîne (FAEE). Ces moléculesmolécules correspondent à une forme de biodiesel peu soluble, hautement énergétique et surtout, peu toxique pour les bactéries. La souche A2A présente un rendement de 9,4 % par rapport à son maximum théorique.
Kay Kiesling fait à nouveau parler de lui dans la revue Nature Biotechnology du 25 mars 2012. En partenariat avec ses collaborateurs, il est parvenu à améliorer la précédente version de sa souche bactérienne en lui ajoutant un système de régulation dynamique de gènesgènes, ou DSRS, impliqués dans la biosynthèse de diesel. Le rendement affiché est maintenant de 28 %, soit trois fois plus qu'avant. Cette évolution conséquente mérite quelques explications.
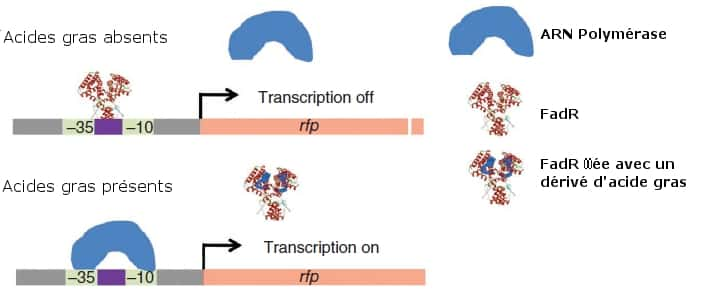
Le système de régulation dynamique de gènes se compose d'un facteur de transcription nommé FadR. En présence d'acides gras, il ne se fixe pas aux promoteurs des gènes intervenant dans la biosynthèse de diesel. Dans le cas inverse, il bloque l'action de l'ARN polymérase. © Adapté de Zhang et al. 2012, Nature Biotechnology
Une production de biocarburant régulée par une protéine
La version 1 de la souche A2A était bridée par deux problèmes. Premièrement, la production des précurseurs pouvait parfois être fortement déséquilibrée, provoquant une synthèse plus importante d'un sous-produit par rapport à l'autre. L'énergie utilisée était alors gaspillée. De plus, de trop fortes concentrations de produits intermédiaires pouvaient être toxiques pour les cellules. Deuxièmement, certaines bactéries utilisaient en priorité les acides gras pour la production de carburant, négligeant d'en conserver pour leur propre métabolismemétabolisme et surtout leur croissance.
Pour s'affranchir de ces limites, les chercheurs ont ajouté dans les cellules des gènes codant pour un système dynamique de |ab132fcd17fbf9e0c0404949199a093c|-régulateur génétiquegénétique sensible à la concentration en acides gras. Il permet de détecter la quantité de tryclycérides présente dans la cellule et de modifier l'expression des gènes intervenant dans la biosynthèse du diesel. L'élément clé du dispositif est un facteur de transcriptiontranscription nommé FadR. Quand des acides gras sont présents, ils se fixent sur la protéineprotéine et empêchent ainsi toute fixation sur des séquences spécifiques de l'ADN. Dans le cas contraire, la présence de FadR sur les zones promotrices de gènes empêche la fixation des ARN polymérasesARN polymérases, bloquant ainsi la biosynthèse de carburant. Seul le retour d'acides gras déverrouille la situation.
Le résultat est là : il n' y a plus de surexpression d'un sous-produit. Par ailleurs, le ralentissement des voies métaboliques impliquées dans la synthèse de biodiesel permet à la cellule de conserver un stock de molécules nécessaire à son bon développement. Un nouveau pas est franchi vers l'exploitation des bactéries pour la production de nos carburants du futur. Le rendement du procédé augmente, le produit final est de bonne qualité et aucune étape de production énergivore n'est requise. Que demander de plus si ce n'est un passage vers une exploitation industrielle ?