au sommaire
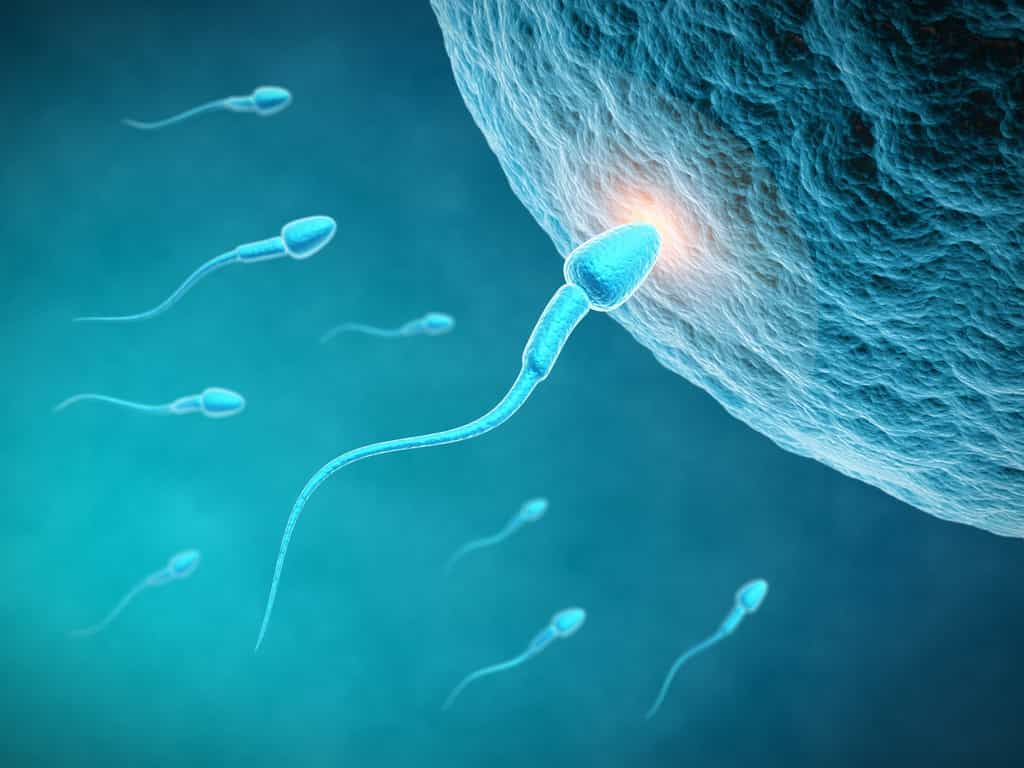
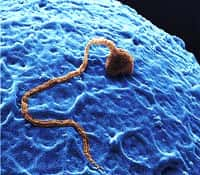
Chez les mammifèresmammifères, les cellules germinales (c'est-à-dire les cellules des organes sexuels : ovule ou spermatozoïde) suivent un cheminement complexe au cours du développement embryonnaire, guidées par des signaux moléculaires. À la puberté, chez les garçons, la méiose permet d'obtenir des cellules germinales haploïdeshaploïdes, les spermatidesspermatides, qui se différencient en spermatozoïdes : c'est la spermatogenèse. Cependant, il arrive que des cellules germinales testiculaires soient incapables de réaliser une méiose pour former des spermatozoïdes fonctionnels, ce qui peut être une cause d'infertilitéinfertilité.
Un des objectifs des recherches en biologie de la reproduction est de recréer le développement des cellules germinales in vitroin vitro. Dans ce cadre, une étape importante a été franchie par des chercheurs chinois qui ont généré des gamètesgamètes mâles fonctionnels à partir de cellules souches embryonnaires de souris.
Lors de ces travaux parus dans Cell Stem Cell, l'équipe a exposé des cellules souches embryonnaires de souris à un cocktail de moléculesmolécules pour les transformer en cellules germinales primordiales. Les chercheurs ont adapté un protocoleprotocole déjà publié qui utilisait un milieu (N2B27) contenant un précurseur de l'acideacide rétinoïque (la vitamine Avitamine A) et de l'insulineinsuline. Ensuite, les chercheurs ont mimé l'environnement tissulaire des cellules germinales précurseurs en les cultivant avec des cellules de testiculetesticule et des hormoneshormones sexuelles. Ils ont trouvé que la différenciation des cellules in vitro nécessitait l'exposition simultanée aux hormones sexuelles testostéronetestostérone et FSHFSH et à l'extrait d'hypophysehypophyse bovine (BPE).

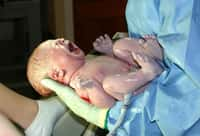
Des bébés souris en bonne santé sont nés. Ils ont ensuite donné naissance à une nouvelle génération. © Zhou et al., Cell Stem Cell 2016
La gamétogenèse réalisée in vitro donne des spermatides fonctionnelles
De plus, l'exposition à l'activine A, à des facteurs appelés BMP et à l'acide rétinoïque permettait d'initier la méiose et des changements d'expression génétiquegénétique ressemblant à ceux observés in vivoin vivo dans des cellules germinales. Dans ces conditions, les cellules ont pu réaliser leur méiose et ont permis d'obtenir des cellules proches de spermatozoïdes, avec un contenu chromosomique correct. Cependant, les cellules générées au laboratoire n'étaient pas des spermatozoïdes complètement différenciés : il s'agissait plutôt de spermatides, les cellules haploïdes issues de la méiose qui deviennent spermatozoïdes.
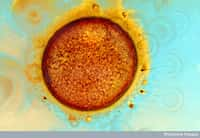
Pour montrer que ces spermatides étaient fonctionnelles, les chercheurs les ont injectées dans des ovocytesovocytes de souris, par injection intracytoplasmique (ICSIICSI), et ont transféré les embryons chez des souris femelles. Les embryonsembryons se sont développés correctement : la descendance était en bonne santé et fertile et a donné naissance à la génération suivante.
Cependant, avant que cette technique soit utilisée en clinique, des questions éthiques devront être considérées, même si Jiahao Sha, de l'université médicale de Nanjing, un des auteurs de ces travaux, semble enthousiaste quant à l'avenir de cette technique : « Si elle s'avère sûre et efficace chez l'Homme, notre plateforme pourrait potentiellement générer des spermatozoïdes entièrement fonctionnels pour l'insémination artificielleinsémination artificielle ou pour les techniques de fécondation in vitro. Parce que les traitements actuellement disponibles ne fonctionnent pas pour de nombreux couples, nous espérons que notre approche pourra améliorer considérablement les taux de réussite pour l'infertilité masculine ».