au sommaire
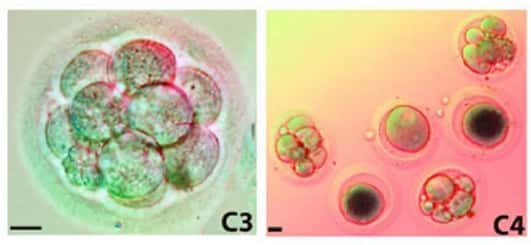
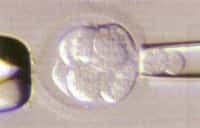
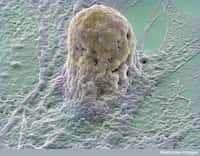
Des blastocystes humains dont les noyaux sont ceux des cellules d'un donneur. Crédit Andrew French et al.
Un pas de plus vers le clonage humain vient d'être franchi si l'on en croit les résultats, spectaculaires, qui viennent d'être publiés dans la revue scientifique Stem Cells. Les six auteurs travaillent pour trois entreprises privées, Stemagen, Genetics Institut et The Reproductive Sciences Center et prétendent avoir obtenu cinq embryons, dont au moins trois clones, à partir d'ovocytes (dont le destin est de devenir ovules) et de cellules de peau prélevées chez des hommes adultes. La technique décrite dans leur publication n'est pas une nouveauté : appelée Transfert nucléaire de cellules somatiquescellules somatiques (Somatic Cell Nuclear Transfer, SCNT), elle a connu son heure de gloire avec la brebis Dolly, née en 1996 (et morte en 2003).
Elle consiste à prélever sur l'animal à cloner le noyau d'une cellule somatique (c'est-à-dire une cellule du corps et non de la lignée reproductive, comme les ovules et les spermatozoïdesspermatozoïdes) puis à le glisser dans un ovocyte dont on a préalablement retiré le noyau. Celui-ci contenant les chromosomeschromosomes, l'organisme obtenu, s'il veut bien se développer, est un clone génétiquegénétique de l'animal dont on a prélevé un noyau.
Dans le cas des animaux d'élevage, l'idée est vraiment de cloner des individus. Pour l'homme, l'objectif est de produire des embryons à un stade très précoce (appelé blastocysteblastocyste, ou blastula) dont on prélèvera des cellules souchescellules souches, capables, espère-t-on, de régénérer un tissu lésé. Mais les primatesprimates semblent plus rétifs que les brebis à cette technique. En novembre 2007, toutefois, une équipe américaine annonçait la réussite chez le macaque.
Terrain miné
Chez l'homme, une équipe de la Newcastle University (Royaume-Uni) avait obtenu des embryons en 2005, mais à partir de cellules issues d'embryons et non de donneurs adultes. L'un des chercheurs, Miodrag Stojkovic, a depuis quitté l'équipe avec fracas. En 2004, le coréen Hwang Woo-suk avait annoncé la réussite du clonage humain et la production de cellules souches mais avait ensuite été convaincu de fraude. Toutefois, il semble bien que le chercheur coréen soit parvenu à cloner Snuppy, un lévrier afghan.
Le terrain sur lequel s'aventurent les six chercheurs américains qui défraient la chronique aujourd'hui est donc difficile et miné. Les travaux publiés dans Stem Cells sont également accessibles, librement, sur le site InternetInternet de Stem Cells Express, sous forme d'un résumé et, pour l'article compet, d'un document PDF. Tout le monde peut donc se pencher sur le mode opératoire. L'équipe a prélevé chez trois jeunes femmes (20 à 24 ans) 29 ovocytes mûrs qui ont ensuite énucléés (l'article scientifique précise que ces ovocytes ont été donnés sans contrepartie financière, ce qui aurait constitué un délit). Les chercheurs ont ensuite prélevés chez deux hommes quelques cellules de peau (des fibroblastesfibroblastes plus précisément), dont les noyaux ont été extraits et introduits dans les ovocytes.
Sur ces 29 œufs, cinq ont donné des embryons au stade blastocyste. Les chercheurs les ont alors détruits pour vérifier que leurs chromosomes étaient strictement identiques à ceux des cellules des donneurs et donc qu'il s'agissait bien de clones. La preuve n'a pu être apportée que pour trois d'entre eux. Mais il s'agit bien d'une première.
Puisque les noyaux proviennent de donneurs adultes (et non d'embryons comme dans l'expérience de la Newcastle University), on peut envisager des applicationsapplications de médecine dite régénérative. Pour réparer une lésion grave, on prélèverait quelques cellules de peau que l'on transformerait par clonage en blastocystes puis en lignées de cellules souches. Celles-ci pourraient alors être installées au niveau de la lésion, sans risque de rejet puisque leur ADNADN serait celui du patient. Comme elles savent le faire, ces cellules indifférenciées pourraient se transformer et devenir similaires aux cellules environnantes, reconstituant le tissu disparu.
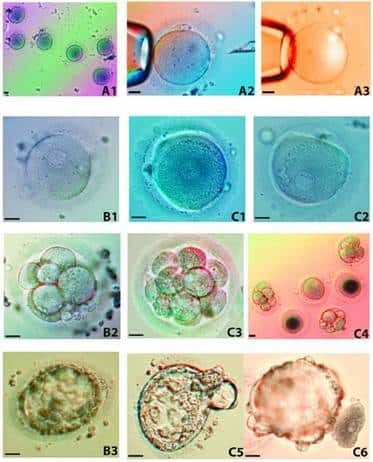
Différentes phases de l'expérience. A1 : ovocytes. A2 : énucléation à la pipette. A3 : la même chose, vue en UV. B1 à B3 : premiers stades du développement parthénogénétique (ces œufs n'ont pas reçu de noyaux
des donneurs). C1 à C6 : embryogénèse après introduction des noyaux provenant des cellules des donneurs.
© Andrew J. French, Catharine A. Adams, Linda S. Anderson, John R. Kitchen, Marcus R. Hughes,
Samuel H. Wooda
Encore une étape à franchir
Il reste à pousser l'expérience jusqu'à l'obtention de cellules souches, ce que l'équipe n'a volontairement pas fait afin de vérifier qu'il y a bien eu clonage du matériel génétiquematériel génétique. « Nous aurions adoré atteindre ce Saint-Graal et créer une lignée de cellules souches, a confié à la revue Nature Andrew French, de Stemagen, principal auteur de l'étude. Mais nous voulions d'abord terminer la première étape. »
Les réactions commencent seulement à éclore dans la communauté scientifique et ailleurs. Le Vatican a condamné la destruction de blastocystes. Miodrag Stojkovic, relecteur de la revue Stem Cells, a félicité les auteurs et affirme qu'il y a une « différence énorme » avec les travaux auxquels il a participé à la Newcastle University. Robert Lanza, qui travaille dans une société concurrente, Advanced Cell Technology, émet des doutes sur l'état de santé des embryons obtenus. Mais l'intérêt est manifestement grand. A l'heure où nous écrivons ces lignes, le site Web de Stemagen est inaccessible...