au sommaire
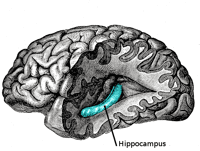
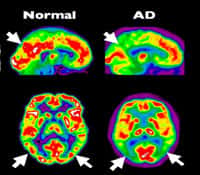
La maladie d’Alzheimer, caractérisée par des pertes de mémoire et un déclin manifeste des aptitudes cognitives, est entre autre marquée par la diminution de la taille de l'hippocampehippocampe, une structure profondément enfouie dans le cerveau qui stocke les souvenirs. À partir de 65 ans, le risque de déclencher la première maladie neurodégénérative mondiale est multiplié par deux. Mais pour un certain nombre d'individus, les probabilités pourraient encore être plus fortes.
Une première étude parue dans la revue Nature Genetics vient de montrer en effet que certaines versions mutées de plusieurs gènes pouvaient accélérer le vieillissement du cerveau (de quatre ans en moyenne) et favoriser la régression de l'hippocampe.
Le chromosome 12 fait régresser l’hippocampe
Ces résultats, les scientifiques les doivent à l'analyse par IRM de 9.232 participants volontaires de huit grandes cohortes européennes et nord-américaines, âgés de 56 à 84 ans (67 ans de moyenne). En tout, 46 variations génétiquesgénétiques ont été répertoriées sur quatre gènes différents. Deux d'entre eux sont portés par le chromosomechromosome 12 (12q14 et 12q24), sur lequel ont été repérées 18 mutations associées de manière significative à la régression de l'hippocampe. Les autres variants génétiques sont positionnés sur les chromosomes 2 et 9 (sur ce dernier, il s'agissait d'individus plus jeunes).
La mutation dite rs7294919 était le plus fortement corrélée à la diminution de volumevolume. Se produisant au niveau du gène HKR (responsable de l'apoptoseapoptose, ou mort programmée des cellules), elle n'est que la substitution d'une cytosinecytosine par une thyminethymine dans la longue séquence ADNADN. Les autres gènes touchés jouent un rôle dans le développement embryonnaire (WIF1), dans le diabètediabète (DPP) ou la migration neuronale (ASTN2).
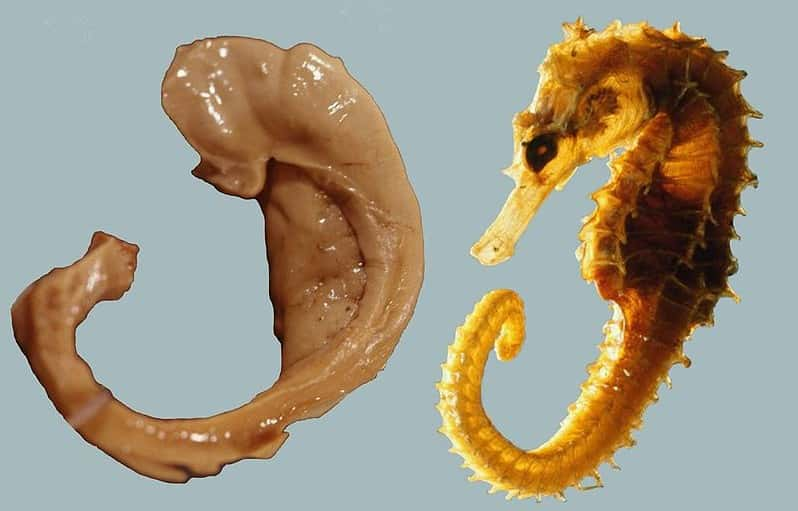
La ressemblance frappante entre la région qui stocke la mémoire et l'hippocampe peuplant les océans, on comprend d'où vient son nom. Comme le poisson syngnathidé qui vit sur le fond de l'océan, cette zone du cerveau se trouve profondément enfouie sous d'autres structures. © Professeur Laszlo Seress, Wikipédia, cc by sa 3.0
Les biologistes ignorent précisément les mécanismes qui amènent cette dégénérescence de l'hippocampe. Une explication partielle est que le gène HKR affecte négativement le développement ou la duréedurée de vie de neuronesneurones du siège de la mémoire, les faisant disparaître de manière plus précoce. Dans ce cas, une version saine permettrait une conservation plus longue de cette structure du cerveau si importante.
Cette recherche pourrait avoir des répercussions cliniques à long terme aussi bien sur le vieillissement cérébral naturel que sur la maladie d'Alzheimermaladie d'Alzheimer. Ces gènes ne sont pas directement impliqués dans la neurodégénérescence, mais peuvent prédisposer à une forme plus sévère et plus précoce. En effet, la maladie s'attaque également à l'hippocampe. Si celui-ci a déjà été attaqué et abîmé, l'accélération sera d'autant plus forte.
Des gènes qui limitent la taille du cerveau… et l’intelligence
Une seconde étude, parue le même jour dans la même revue, confirme certains de ces résultats mais aborde également d'autres points. Si rs7294919 est bien corrélé avec la perte de l'hippocampe (cette fois sur 21,151 personnes), la mutation rs10784502 sur le gène HMGA2 (lui aussi sur le chromosome 12) serait directement liée au volume intracrânien et au QI.
Avec cette fois 15.782 cobayes, ils se sont rendu compte là encore qu'un changement d'un seul nucléotidenucléotide pouvait diminuer l'espace dans lequel le cerveau est contenu (comblé vers l'âge de 20 an seulement). Les personnes dotées de ce variant réalisaient des performances inférieures aux tests de QI, suggérant implicitement que la taille du cerveau peut effectivement jouer un rôle dans l'intelligence. Mais ce n'est pas le seul facteur (les connexions entre neurones sont fondamentales, comme l'expérience passée).
Avec ces recherches, le cerveau dévoile quelques-uns de ses nombreux mystères. Malgré tout, ces travaux sont encore bien théoriques et les applicationsapplications pratiques et cliniques qui en découleront ne sont pas pour demain. Néanmoins, elles présentent un sérieux intérêt car la démencedémence est grandissante dans le monde entier, avec l'allongement de la durée de vie. La ralentir, comme cela pourrait être la cas avec des thérapiesthérapies adaptées, serait déjà un énorme pas en avant.