au sommaire
Nous semblant banale, l'activité photosynthétique des plantes a une longue histoire évolutive derrière elle et repose même, peut-être, sur des phénomènes quantiques allant bien au-delà de la chimiechimie de base. Cette histoire nous intéresse parce que les plantes produisent l'oxygène que nous respirons et qui a joué, il y a longtemps, un rôle majeur dans l'évolution des formes de vie. Grâce à cet élément chimiqueélément chimique offrant une source d'énergieénergie pour qui sait respirer, des organismes multicellulaires, plantes et animaux, ont pu grandir et se complexifier.
Les premiers organismes photosynthétiques semblent être apparus il y a plusieurs milliards d'années. Mais, initialement, ils ne devaient pas produire d'oxygène et devaient donc ressembler aux bactériesbactéries pourpres et vertes sulfureuses actuelles, effectuant donc une photosynthèse anoxygénique. Ce n'est que plus tard que seraient apparues des cyanobactéries constructrices de stromatolites, avec une photosynthèse dégageant de l'oxygène, sans doute à l'époque un poison pour de nombreux organismes.
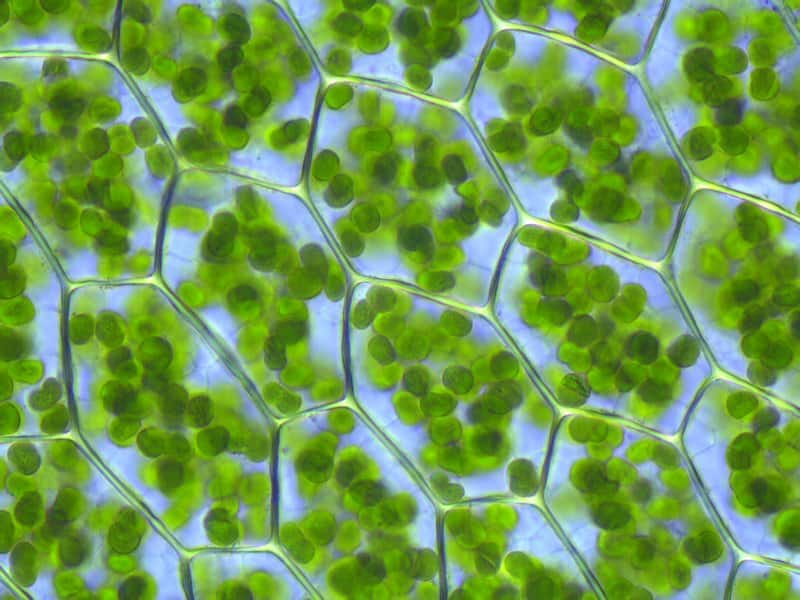
Les chloroplastes sont le lieu de la photosynthèse des végétaux. Ils sont ici très visibles, à l'intérieur de cellules végétales. © Kristian Peters, Wikimedia, CC by-sa 3.0
Les chloroplastes sont d'anciennes cyanobactéries
D'abord présente chez des bactéries, la photosynthèse oxygénique serait ensuite apparue dans les cellules des plantes, des eucaryoteseucaryotes, donc différentes des bactéries, selon un des chemins qu'emprunte l'évolution de la vie : la symbiose. Les actuels chloroplastes, présents dans les cellules des grandes algues et des plantes, seraient en fait les descendants de bactéries qui auraient scellé une sorte de partenariat avec les cellules eucaryotes, qui leur apportaient le gîte et le couvert en échange de la production de sucressucres.
De bons arguments valident cette hypothèse mais les biologistes cherchent toujours à préciser quand et comment cet évènement serait survenu. Pour résoudre des énigmes de ce genre, ils disposent aujourd'hui des outils de plus en plus performants de la génomiquegénomique, qui permettent de compulser les horloges moléculaireshorloges moléculaires et de préciser les relations phylogénétiquesphylogénétiques entre les êtres vivants. Un groupe de chercheurs, mené par des membres de l'université de Bristol, vient de publier à ce sujet un article intéressant dans les Pnas (Proceedings of the National Academy of Sciences).
Leur analyse montre que les micro-organismesmicro-organismes qui deviendront les chloroplastes ont divergé des cyanobactéries il y a au moins 2,1 milliards d'années et qu'ils vivaient dans l'eau douce ou peu salée. Il aurait fallu ensuite environ 200 millions d'années pour que le mariage par endosymbioseendosymbiose entre les eucaryotes et ces organismes se constitue pleinement. Si les chercheurs ont raison, il faut de plus en conclure que les algues et les autres plantes sont d'abord apparues et ont évolué dans des environnements qui n'étaient pas marins.
La vie aurait inventé la photosynthèse il y a 3,5 milliards d'années...
Article de Laurent SaccoLaurent Sacco publié le le 02/04/2009
L'atmosphèreatmosphère de notre planète ne contient de l'oxygène en grande quantité que depuis 2,5 milliards d'années environ. C'est du moins ce qu'on croyait jusqu'à la publication récente dans Nature d'une nouvelle analyse de roches de la région de Pilbara en Australie. Selon certains géochimistes, l'atmosphère de la TerreTerre était peut-être semblable à celle d'aujourd'hui des centaines de millions d'années plus tôt !
La photosynthèse serait apparue chez certains organismes primitifs entre 2.800 et -2.400 millions d'années si l'on en croit certaines archives géologiques terrestres. Mais certains la font remonter bien plus tôt en faisant l'hypothèse que les stromatolitesstromatolites retrouvées dans des couches plus anciennes encore sont le produit d'une activité biologique. Actuellement, nous n'en sommes sûrs que pour ceux datant de -2.724 millions d'années mais des stromatolites existaient déjà sur Terre il y a 3,5 milliards d'années environ.
Quoi qu'il en soit, une certitude demeure, concernant les immenses dépôts de ferfer du bassin de Hamersley en Australie. Ils datent de l'époque du Sidérien alors que la surface des continents était devenue suffisamment importante pour que se forment des mers peu profondes entourées de grande plates-formes continentales. Les conditions étaient remplies pour que de grands tapis de bactéries construisent des stromatolites en quantités importantes et dégagent massivement de l'oxygène par photosynthèse.
Ce gazgaz corrosif a alors pu oxyder le fer en solution dans les océans et entraîner sa précipitation sous forme d'hydroxyde de fer, de carbonate de fer, de silicatesilicate ou de sulfuressulfures, selon des variations de l'acidité et du degré d'oxydoréductionoxydoréduction de l'eau de mer.
C'est ce qu'on appelle la Grande oxydationGrande oxydation ou la Catastrophe de l'oxygène.
Vers -1.900 millions d'années, la presque totalité du fer présent dans les océans avait précipité et il se retrouve aujourd'hui dans les grands gisementsgisements de mineraiminerai mondiaux tels que ceux de Hamersley. La production d'oxygène par les stromatolites ne s'est pas arrêtée pour autant et les océans ont commencé à relâcher ce gaz dans l'atmosphère, qui a atteint rapidement un taux de 15 % de la valeur actuelle.
C'est du moins le scénario standard accepté par la communauté des géochimistes. Un groupe de géologuesgéologues avec parmi eux le géochimiste Hiroshi Ohmoto de l'université de Penn State pense qu'il faut revoir cette hypothèse, comme ils viennent de l'expliquer dans un article de Nature Geoscience.

Les formations rubanées du craton de Pilbara dans la partie ouest de l'Australie. © Hiroshi Ohmoto/Yumiko Watanabe
Une couche oxydée très épaisse et à grande profondeur...
Ils se fondent sur les analyses récentes de dépôts de jaspe rouge trouvés dans la région du cratoncraton de Pilbara en Australie. Ce minéralminéral est une roche sédimentaireroche sédimentaire contenant de 90 à 95 % de silicesilice, souvent classée avec les quartzquartz microcristallins, et parfois constituée de radiolairesradiolaires calcédonieux pris dans un cimentciment de calcédoine. Les forages effectués dans ces couches ont permis de montrer qu'elles étaient associées à des évents hydrothermaux comparables à ceux que l'on connaît actuellement au fond des océans comme ceux de la Cité perdue.
Parce qu'il est riche en hématitehématite, un minéral composé d'oxyde de fer III de formule Fe2O3, on pensait que ce jaspe provenait d'une oxydation ultérieure des roches exposées à l'airair libre ou au moins installées sous des couches d'eau peu profondes alors que l'atmosphère de la Terre était devenue riche en oxygène. Les roches de Pilbara datent en effet de -3,46 milliards d'années donc bien avant la Grande Oxydation.
Un premier problème s'est posé quand les chercheurs se sont rendu compte que les forages indiquaient une trop grande épaisseur de jaspe rouge pour qu'il soit le produit d'une altération de surface. Or, on observe aujourd'hui que des composés riches en fer flottant à la surface de l'océan se transforment en oxydes sous la seule action des rayons UVUV et donc sans nécessairement que l'eau ni l'atmosphère soient riches en oxygène.
Lorsqu'ils ont coulé au fond, sous forme de petites particules, il a suffi que ces oxydes soient chauffés par des évents hydrothermaux à plus de 100 °C pour que de l'hématite apparaisse. La présence d'un grand nombre de couches peut donc s'expliquer par un processus continu de déposition de ces particules. Mais cette hypothèse devait être testée.
Il se trouve qu'une observation au microscope électroniquemicroscope électronique permet de savoir s'il s'agit d'agrégats de petits grains d'hématite ou bien de grands cristaux ayant précipité dans une eau riche en oxygène. La seconde hypothèse s'est révélée être la bonne et elle a des implications fascinantes...
Personne ne doute que les couches ont bien 3,46 milliards d'années. Cela implique donc, qu'à cette époque, elles se sont formées à partir du contact de fluides riches en fer et chauds avec de l'eau de mer chargée d'oxygène... et le tout à grande profondeur !
On ne peut alors que difficilement échapper à la conclusion que, non seulement les océans entiers de la planète étaient eux-mêmes riches en oxygène mais probablement aussi à saturation, ce qui implique un dégazagedégazage important et une atmosphère contenant de l'oxygène en grande quantité il y a 3,46 milliards d'années.
La découverte de la photosynthèse par la vie serait donc ancienne et cette conclusion colle parfaitement avec l'âge des plus anciens stromatolites connus qui, rappelons-le, sont datés de 3,5 milliards d'années environ. En allant encore plus loin, cela suggère que les traces de résidus carbonés que certains interprètent comme résultant d'une activité biologique il y a -3,8 milliards d'années, en raison de leur enrichissement inhabituel en 12C, sont bien des preuves de la présence de la vie et de la photosynthèse à cette époque reculée.
Ce qu’il faut
retenir
- Les chloroplastes à l'intérieur des cellules végétales sont probablement issus de bactéries photosynthétiques, ce qui est connu depuis longtemps.
- Les horloges moléculaires indiquent que cette endosymbiose est ancienne, peut-être plus de 2,1 milliards d'années, et qu'elle aurait débuté dans l'eau douce.
- Les algues n'auraient alors colonisé le milieu marin que plus tard, avant de se diversifier il y a environ 800 millions d'années.
























